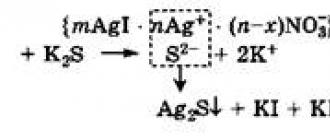Лиофобные коллоидные растворы, как термодинамически неустойчивые системы, могут разрушаться самопроизвольно или под влиянием внешних воздействий. Разрушение коллоидных растворов начинается с их коагуляции.
Коагуляцией называется процесс слипания коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости.
В результате коагуляции укрупненные частицы дисперсной фазы легко седиментируют, и происходит расслоение системы. Таким образом, причиной коагуляции является потеря агрегативной устойчивости коллоидным раствором, а следствием коагуляции - уменьшение его седиментационной устойчивости.
Практически коагуляцию можно вызвать различными внешними воздействиями: добавлением небольших количеств электролита, концентрированием коллоидного раствора, изменением температуры, действием ультразвука, электромагнитного поля и др.
Явление коагуляции лежит в основе многих патологических процессов, протекающих в живых системах. Коагуляция коллоидных растворов фосфата кальция и холестерина в крови приводит к образованию осадков и отложению их на внутренней поверхности кровеносных сосудов (атеросклеротические изменения сосудов).
Коагуляция проявляется в процессе свертывания крови. Свертывание крови играет в организме две противоположные роли: с одной стороны, уменьшает потерю крови при повреждении ткани, с другой - вызывает образование тромбов в кровеносной системе. Свертывание крови - очень сложный ферментативный процесс. Одновременно в крови действует антисвертывающая система, основой которой является гепарин - антикоагулянт крови.
Природу крови необходимо учитывать при ее консервировании. Так как свертыванию крови способствуют катионы кальция, то их удаляют из крови, предназначенной для консервирования, используя различные физико-химические способы. Например, добавка цитрата натрия переводит кальций в осадок, после чего кровь сохраняется в охлажденном состоянии, оставаясь пригодной для переливания в течение 30 суток. Цельную кровь можно декальцинировать также методом ионообмена, используя для этого Na-катиониты.
Коагуляция под действием электролитов . В биологических системах наибольшее практическое значение имеет коагуляция при добавлении небольших количеств электролита, поскольку коллоидные растворы клеток и биологических жидкостей находятся в соприкосновении с электролитами. Коагуляцию коллоидного раствора может вызвать любой электролит. Однако для каждого электролита необходима своя минимальная концентрация, называемая порогом коагуляции (С пк).
Порогом коагуляции называется минимальное количество электролита, которое надо добавить к коллоидному раствору, чтобы вызвать явную коагуляцию (заметную на глаз) - помутнение раствора или изменение его окраски. Порог коагуляции можно рассчитать по формуле:
где Сэл - исходная концентрация раствора электролита; Vэл - объем раствора электролита, добавленного к коллоидному раствору; Vкp -объем коллоидного раствора.
Величина, обратная порогу коагуляции, называется коагулирующим действием (у): у=1/Спк
Коагулирующее действие электролитов на коллоидные растворы с ионным стабилизатором подчиняется правилу Шульце-Гарди : коагуляцию коллоидных растворов вызывают любые ионы, которые имеют знак заряда, противоположный заряду гранул. Коагулирующее действие ионов (у) тем сильнее, чем выше заряд иона-коагулянта.
Коагулирующее действие иона-коагулянта прямо пропорционально его заряду в шестой степени: у = f(z 6). Например, коагуляция золя AgI с отрицательно заряженными гранулами (потенциалопределяющие ионы - анионы I -) происходит за счет действия положительно заряженных ионов. Поэтому при добавлении к этому золю растворов NaCl, CaCl 2 , AlCl 3 коагулирующее действие катионов Na + , Са 2+ , А1 3+ будет резко возрастать; y(Na +):у(Са 2+):у(Аl 3+) = 1:64:729. Коагуляция золя AgI с положительно заряженными гранулами (потенциалопределяющие ионы-катионы Ag +), наоборот, идет за счет отрицательно заряженных ионов. Добавление к золю растворов КCl, K 2 SO 4 , К 3 вызовет увеличение коагулирующего действия анионов в следующем порядке: у(Сl -):y(SO 4 (2-)):y 3- = 1:64:729.
От правила Шульце-Гарди встречаются отклонения, поскольку на коагулирующее действие иона кроме заряда влияют радиус коагулирующего иона, а также природа иона, сопутствующего иону-коагулянту.
Сильное влияние электролита на коагуляцию коллоидных растворов следует учитывать при введении растворов солей в живые организмы. При этом имеет значение не только концентрация, но и заряд вводимых ионов. Так, физиологический раствор хлорида натрия (0,9%) нельзя заменить изотоническим раствором сульфата магния, поскольку в этой соли имеются двухзарядные ионы Mg 2+ и SО 4 (2-), обладающие более высоким коагулирующим действием, чем ионы Na + и Сl - .
При инъекциях электролита в мышечную ткань или кровь человека необходимо вводить его постепенно, медленно, чтобы не вызвать коагуляцию биологических коллоидных систем. Быстрое введение электролита из-за малой скорости диффузии его в крови или мышечной ткани приводит к накоплению электролита, локальному (местному) превышению его пороговой концентрации и вызывает коагуляцию биосубстратов, которую трудно остановить. При медленном введении электролит успевает уноситься с током крови и диффундировать в соседние ткани, поэтому пороговая концентрация не достигается и коагуляция не наступает. Это явление в живых тканях называется «привыканием».
Механизм коагуляции . Роль электролитов при коагуляции заключается в уменьшении расклинивающего давления между сближающимися коллоидными частицами. Это может происходить двумя путями: за счет уменьшения заряда поверхности твердой фазы (заряда поверхности ядра), т.е. за счет снижения межфазного потенциала Ф мф, или за счет уменьшения толщины (сжатия) ионных атмосфер мицелл при неизменном заряде поверхности их ядер. В связи с этим возможны два вида коагуляции: нейтрализационная и концентрационная.
Нейтрализационная коагуляция наступает под действием электролита, который химически взаимодействует с потенциалопределяющими ионами, связывая их в прочное соединение (например, переводя в осадок) и тем самым уменьшая заряд поверхности ядра. Нейтрализационная коагуляция наблюдается, например, при добавлении K 2 S к коллоидному раствору AgI с положительно заряженными гранулами (потенциалопределяющие ионы - катионы Ag +). Между коагулирующими анионами S 2- и потенциалопределяющими катионами Ag + происходит реакция с образованием малорастворимого соединения Ag 2 S, что приводит к разрушению мицеллы AgI:

В результате связывания потенциалопределяющих катионов Ag + межфазный потенциал Ф мф падает и число противоионов NO 3 (-), необходимых для компенсации заряда поверхности ядра, уменьшается. Таким образом, ионные атмосферы вокруг ядер становятся тоньше, снижается расклинивающее давление между сближающимися частицами, а это в свою очередь приводит к их слипанию в более крупные агрегаты.
Концентрационная коагуляция наступает под действием электролита, который химически не взаимодействует с ионами стабилизатора и не изменяет заряд поверхности ядра мицеллы. Однако в этом случае коагулирующее действие проявляют те ионы добавленного электролита, которые являются противоионами для данных мицелл, так как за счет повышения их концентрации они проникают внутрь гранулы, сжимая (уплотняя) ионную атмосферу мицеллы вокруг ядра. Концентрационная коагуляция происходит при неизменном межфазном потенциале Ф мф, но сопровождается, как правило, уменьшением ζ-потенциала. Концентрационная коагуляция наблюдается, например, при добавлении нитратов к коллоидному раствору AgI, мицеллы которого содержат противоионы NО 3 (-):

По мере увеличения концентрации добавляемых ионов NO 3 (-) они способствуют внедрению противоионов диффузного слоя в адсорбционный слой. При этом диффузный слой сжимается, и может наступить такое состояние, при котором диффузный слой исчезнет вовсе и гранула станет электронейтральной. В таком состоянии расклинивающее давление между сближающимися частицами минимально, и это приводит к слипанию частиц в более крупные агрегаты.
Поскольку заряд гранул в этих условиях равен 0, то в электрическом поле они не приобретают направленного движения к электродам, так как гранула находится в изоэлектрическом состоянии.
Изоэлектрическим состоянием называется состояние коллоидных частиц, при котором электрокинетический потенциал ζ равен 0 и которое характеризуется отсутствием направленного движения гранул в электрическом поле.
В агрегативно-устойчивом состоянии коллоидного раствора значение колеблется в пределах 50-70 мВ. При уменьшении ζ-потенциала под действием электролита до 25-30 мВ в системе не наблюдается никаких внешних изменений (помутнения или изменения окраски), так как скорость коагуляции еще очень низкая, вследствие чего эта стадия (I) коагуляции называется «скрытой» коагуляцией (рис. 6.10). Дальнейшее добавление электролита свыше Спк вызывает еще большее сжатие диффузного слоя и уменьшение ζ-потенциала, что сопровождается помутнением раствора, и начинается «явная» коагуляция. Вначале скорость коагуляции быстро увеличивается (стадия II), а затем становится постоянной, когда значение ζ-потенциаластанет равным нулю и наступит стадия быстрой коагуляции (III).
Коагуляция смесями электролитов. На практике коагуляция часто вызывается действием смеси электролитов. При этом существует три возможных варианта взаимодействия между электролитами: аддитивное действие, антагонизм и синергизм.
Рис. 6.10. Влияние концентрации электролитана скорость коагуляции
Аддитивность - это суммирование коагулирующего действия ионов, вызывающих коагуляцию.
Аддитивное действие проявляется в тех случаях, когда электролиты, содержащие коагулирующие ионы, не взаимодействуют химически между собой. Например, смесь солей КСl и NaNО 3 проявляет аддитивное действие по отношению к коллоидным растворам как с отрицательно, так и с положительно заряженными гранулами. В первом случае коагуляцию вызывают катионы К + и Na + , во втором - анионы Сl - и NO 3 (-).
Антагонизм - это ослабление коагулирующего действия одного электролита в присутствии другого.
Pb 2+ + 2Cl - = PbCl 2 ↓
Антагонизм действия наблюдается в тех случаях, когда в результате химической реакции между электролитами коагулирующие ионы связываются в нерастворимое соединение (выпадают в осадок) либо в прочный комплекс, который не обладает коагулирующей способностью. Например, коагулирующее действие катионов Рb 2+ по отношению к отрицательно заряженным гранулам ослабляется в присутствии NaCl, так как протекает реакция, в результате которой уменьшается концентрация коагулирующих ионов Рb 2+ в растворе из-за выпадения в осадок РbСl 2:
Синергизм - это усиление коагулирующего действия одного электролита в присутствии другого.
Синергизм действия возможен, когда между электролитами происходит химическое взаимодействие, в результате которого образуется многозарядный ион, обладающий очень высокой коагулирующей способностью. Например, коагулирующее действие FeCl 3 и KCNS по отношению к положительно заряженным гранулам (коагулирующие ионы Сl(-) и CNS -) усиливается во много раз, так как происходит реакция, в результате которой образуются многозарядные анионы 3- , проявляющие высокую коагулирующую способность:
FeCl 3 + 6KCNS → K 3 + 3KCl
Используя электролиты в лабораторной и медико-санитарной практике, необходимо всегда учитывать возможность коагуляции в биологических средах. Так, при введении различных лекарственных веществ в организм (в виде инъекций) следует предварительно убедиться в том, что эти вещества не являются синергистами, чтобы избежать возможной коагуляции. С другой стороны, при очистке промышленных вод вредным может оказаться антагонизм вводимых электролитов, препятствующий разрушению коллоидных загрязнений.
В природных водах, как и в промышленных сточных водах, коагуляция нередко происходит в результате смешивания дисперсных систем, содержащих разнородные частицы. Гетерокоагуляцией называется коагуляция коллоидных растворов, содержащих разнородные частицы, отличающиеся по химической природе, знаку или величине заряда.
Частным случаем гетерокоагуляции является взаимная коагуляция - слипание разноименно заряженных гранул коллоидных растворов. При этом коагуляция происходит тем полнее, чем полнее нейтрализуются заряды гранул.
Гетерокоагуляции широко используется на практике в связи с проблемой очистки природных и промышленных вод. В воду, содержащую коллоидные примеси, добавляют соли алюминия или железа (3), которые являются хорошими коагулянтами. Эти соли в результате гидролиза дают малорастворимые гидроксиды Аl(ОН) 3 или Fe(OH) 3 , образующие коллоидные растворы с положительно заряженными гранулами. В результате происходит коагуляция, сопровождающаяся образованием хлопьев из агрегированных разнородных мицелл, которые выпадают в осадок.
В процессе коагуляции, связанной с потерей агрегативной устойчивости, происходит разрушение коллоидного раствора, сопровождающееся выпадением осадка - коагулята. Однако, если коагуляту возвратить агрегативную устойчивость, то может произойти обратный процесс - пептизация.
Пептизацией называется процесс, обратный коагуляции - превращение осадка, образовавшегося в результате коагуляции, в устойчивый коллоидный раствор.
Пептизация может проводиться двумя путями, каждый из которых приводит к увеличению агрегативной устойчивости за счет восстановления достаточно рыхлых ионных атмосфер у мицелл:
· промыванием коагулята чистым растворителем (дисперсионной средой), что приводит к вымыванию из системы ионов, вызвавших коагуляцию, и разрыхлению ионных атмосфер вокруг частиц;
· добавлением специального электролита-пептизатора, ионы которого, адсорбируясь на поверхности частиц коагулята, восстанавливают рыхлые ионные атмосферы вокруг этих частиц и способствуют переходу их в коллоидное состояние.
Однако не всякий полученный при коагуляции осадок поддается пептизации. Важнейшие условия эффективной пептизации заключаются в следующем:
· к пептизации способны только свежеполученные осадки, так как увеличение продолжительности контакта частиц дисперсной фазы между собой приводит к постепенному уплотнению осадка и вытеснению жидкой фазы из его структуры;
· необходимо добавление небольших количеств электролита-пептизатора, в ином случае может вновь наступить коагуляция;
· пептизации способствуют перемешивание и нагревание.
Процесс пептизации лежит в основе лечения ряда патологических изменений в организме человека: рассасывания атеросклеротических бляшек на стенках кровеносных сосудов, почечных и печеночных камней или тромбов в кровеносных сосудах под действием антикоагулянтов. При этом необходимо учитывать своевременность введения лекарственных веществ (антикоагулянтов) в кровь: застарелые тромбы в кровеносных сосудах, а также уплотнившиеся камни практически не пептизируются, т.е. не рассасываются.
6.9. Грубодисперсные системы: суспензии, эмульсии, аэрозоли
Грубодисперсные системы делятся на три группы: эмульсии, суспензии и аэрозоли.
Эмульсии – это дисперсные системы с жидкой дисперсионной средой и жидкой дисперсной фазой.
Их можно также разделить на две группы:
1. прямые – капли неполярной жидкости в полярной среде (масло в воде);
2. обратные (вода в масле).
Изменение состава эмульсий или внешнее воздействие могут привести к превращению прямой эмульсии в обратную и наоборот. Примерами наиболее известных природных эмульсий являются молоко (прямая эмульсия) и нефть (обратная эмульсия). Типичная биологическая эмульсия – это капельки жира в лимфе. В химической технологии широко используют эмульсионную полимеризацию как основной метод получения каучуков, полистирола, поливинилацетата и др.
Суспензии – это грубодисперсные системы с твердой дисперсной фазой и жидкой дисперсионной средой.
Особую группу составляют грубодисперсные системы, в которых концентрация дисперсной фазы относительно высока по сравнению с ее небольшой концентрацией в суспензиях. Такие дисперсные системы называют пастами. Например, вам хорошо известные из повседневной жизни зубные, косметические, гигиенические и др.
Аэрозоли – это грубодисперсные системы, в которых дисперсионной средой является воздух, а дисперсной фазой могут быть капельки жидкости (облака, радуга, выпущенный из баллончика лак для волос или дезодорант) или частицы твердого вещества (пылевое облако, смерч).
Коллоидные системы занимают промежуточное положение между грубодисперсными системами и истинными растворами. Они широко распространены в природе. Почва, глина, природные воды, многие минералы, в том числе и некоторые драгоценные камни, – все это коллоидные системы.
Большое значение имеют коллоидные системы для биологии и медицины. В состав любого живого организма входят твердые, жидкие и газообразные вещества, находящиеся в сложном взаимоотношении с окружающей средой. С химической точки зрения организм в целом – это сложнейшая совокупность многих коллоидных систем.
Коллоидные системы подразделяют на золи (коллоидные растворы) и гели (студни).
Большинство биологических жидкостей клетки (цитоплазма, ядерный сок – кариоплазма, содержимое вакуолей) и живого организма в целом являются коллоидными растворами (золями).
Для золей характерно явление коагуляции, т.е. слипания коллоидных частиц и выпадение их в осадок. При этом коллоидный раствор превращается в суспензию или гель. Некоторые органические коллоиды коагулируют при нагревании (яичный белок, клеи) или при изменении кислотно-основной среды (пищеварительные соки).
Гели – это коллоидные системы, в которых частицы дисперсной фазы образуют пространственную структуру.
Гели – это дисперсные системы, которые встречаются вам в повседневной жизни.
Со временем структура гелей нарушается – из них выделяется жидкость. Происходит синерезис – самопроизвольное уменьшение объема геля, сопровождающееся отделением жидкости. Синерезис определяет сроки годности пищевых, медицинских и косметических гелей. Очень важен биологический синерезис при приготовлении сыра, творога.
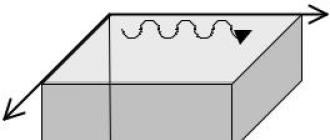
По внешнему виду истинные и коллоидные растворы трудно отличить друг от друга. Чтобы это сделать, используют эффект Тиндаля – образование конуса «светящейся дорожки» при пропускании через коллоидный раствор луча света. Частицы дисперсной фазы золя отражают своей поверхностью свет, а частицы истинного раствора – нет. Аналогичный эффект, но только для аэрозольного, а не жидкого коллоида, вы можете наблюдать в кинотеатре при прохождении луча света от киноаппарата через запыленный воздух зрительного зала.
6.10. Электрокинетические явления в дисперсных системах: электрофорез, электроосмос
Электрический заряд может возникать на любой твердой поверхности, находящейся в контакте с жидкостью. Значение удельного заряда сравнительно небольшое: например, для глины на границе с водой оно составляет несколько десятков милликулонов, поэтому поверхность куска глины массой 1 кг, равная сотым долям квадратного метра, будет иметь ничтожно малый электрический заряд. Частицы глины общей массой 1 кг реализуют поверхность в миллионы раз большую, чем ее сплошной кусок, что приводит к резкому увеличению заряда поверхности. Появление значительного заряда поверхности является причиной возникновения особых электрокинетических явлений, характерных только для дисперсных систем.
Электрокинетическими называют такие явления, которые возникают при воздействии электрического поля на дисперсные системы и в результате перемещения частиц дисперсной фазы или дисперсионной среды. Несмотря на различие электрокинетических явлений все они связаны с наличием двойного электрического слоя и определяются ζ-потенциалом, который именно поэтому и называют электрокинетическим.
Внешнее электрическое поле вызывает такие электрокинетические явления дисперсных систем, как электрофорез и электроосмос.
Электрофорез - это перемещение под действием электрического поля частиц дисперсной фазы относительно дисперсионной среды. Схема электрофореза показана на рис. 6.11, где частица дисперсной фазы для наглядности дана в увеличенном масштабе. При наложении внешнего электрического поля частицы дисперсной фазы начинают двигаться к электроду, знак заряда которого противоположен знаку ζ-потенциала; направление движения частицы на рисунке показано стрелкой.
Движение частиц при электрофорезе обусловлено притяжением разноименных зарядов. Диффузный слой не препятствует взаимодействию разноименных зарядов. Противоионы в этом слое подвижны, распределяются неравномерно и не в состоянии экранировать действие внешнего электрического поля на частицы дисперсной фазы. Движение частиц происходит по границе скольжения.
В процессе электрофореза нарушается сферическая симметрия диффузного слоя противоионов, и он начинает двигаться в сторону, противоположную движению частиц. Противоположно направленный поток частиц диффузного слоя тормозит движение частиц. Этот эффект называют электрофоретическим торможением (короткая стрелка на рис. 6.11).

Рис. 6.11. Схема электрофореза:
При электрофорезе происходит движение частиц дисперсной фазы в направлении силовых линий электрического поля. Электрофорез используют для получения новых материалов, нанесения покрытий, очистки веществ от примесей и выделения продуктов. В медицине электрофорез применяют для введения лекарственных веществ. На кожу пациента накладывают тампон, смоченный раствором лекарственного препарата, а сверху - электроды, к которым приложен низкий, безопасный для организма потенциал. В ходе этой процедуры частички лекарственного препарата под действием электрического поля переходят в ткани организма человека.
Электроосмосом называют перемещение дисперсионной среды под действием внешнего электрического поля (рис. 6.12). Движение дисперсионной среды обусловлено притяжением разноименных зарядов. Оно происходит зачастую в капиллярах и в каналах пористых тел. Когда ζ-потенциал отрицательный, то положительно заряженные противоионы диффузного слоя притягиваются к отрицательному электроду. Противоионы увлекают за собой жидкость, составляющую дисперсионную среду. В результате этого происходит движение жидкости, причем перемещение жидкой дисперсионной среды относительно частиц дисперсной фазы, как и в случае электрофореза, происходит по границе скольжения.

Рис. 6.12. Схема электроосмоса
1 - дисперсная система; 2 - перегородка
Электроосмос используют, например, для обезвоживания древесины и других пористых материалов: строительных, грунта, продуктов питания, сырья для пищевой промышленности и др. Влажную массу помещают между электродами, а вода в зависимости от структуры ДЭС движется к одному из них и собирается в специальной емкости.
Для осуществления электрофореза или электроосмоса необходимо внешнее электрическое поле, т.е. движение частиц при электрофорезе или среды при электроосмосе является следствием воздействия этого поля.
Следует отметить, что явление электрофореза характерно главным образом для коллоидных растворов (золей), т.е. для систем, у которых размеры частиц дисперсной фазы не превышают 0,1 мкм. Электроосмос может наблюдаться не только в отношении коллоидных растворов, которые являются высокодисперсными системами, но и в отношении средне- и грубодисперсных систем.
Коллоиды подразделяются на «лиофильные» и «лиофобные» или же для случая водных золей на «гидрофильные» и «гидрофобные». Стабильность гидрофобных золей зависит большей частью от заряда на частицах, тогда как для гидрофильных золей это обстоятельство менее важно, поскольку частицы стабилизируются посредством «сольватации» или «гидратации».
Коллоидный кремнезем относится к гидрофильным, хотя при некоторых условиях, когда коагуляция частиц вызывается солями, кремнезем отчасти и гидрофобен. Эти термины не столь важны по отношению к кремнезему, за исключением случая, когда предусматривается использование органических флоку - лирующих агентов и адсорбция этих веществ на поверхности Кремнезема превращает ее в поверхность с выраженными гидрофобными свойствами.
Коагуляция рассматривается как результат воздействия вандерваальсовых сил притяжения, которые стягивают вместе две частицы в момент их столкновения, если только этому притяжению не противостоит гидратный барьерный слой или силы электростатического отталкивания между одинаково заряженными частицами, или же обе эти причины. Следовательно, существуют два фактора, которые замедляют коагуляцию кремнезема:
1. Гидратация поверхности частиц посредством образования слоя молекул воды, связанных водородной связью с поверхностными группами SiOH.
2. Отрицательный ионный заряд, возникающий на частицах выше рН - 3,5, и окружающее частицу положительно заряженное облако, состоящее из противоионов - катионов, таких, как Na+, что ведет к образованию «двойного электрического слоя».
Для большинства разбавленных кремнеземных золей при рН~2, когда на частице находится лишь слабый ионный заряд, при воздействии на систему электролитом никакой коагуляции не будет наблюдаться, по-видимому, из-за гидрат - ного слоя. Однако Хардинг обратил внимание на тот факт, что относительно большие по размеру коллоидные частицы кремнезема, диаметром 50-100 нм или более, начинают флокулировать при низких значениях рН, тогда как небольшие частицы еще не подвержены этому процессу. Остается определить, обусловливается ли флокуляция вандерваальсовыми силами притяжения между частицами или же образованием многократных водородных связей между покрытыми силаноль - ными группами поверхностями в пределах области контакта частиц при их столкновении.
В интервале значений "рН 7-10 золи кремнезема стабильны, если концентрация электролита незначительна, но начинают коагулировать при добавлении солей. Таким образом, следует рассмотреть два механизма агрегации:
1. Притяжение частицы к частице за счет действия сил Ван-дер-Ваальса, математическое описание которых выполнено Лондоном и распространено впоследствии на коллоидные частицы Гамакером .
2. «Связывание» мостиковой связью двух частиц под действием флокулирующего или коагулирующего агента.
В первом случае притяжение ведет к коагуляции, когда силы отталкивания между частицами, несущими сходные ионные заряды, понижаются посредством добавления солевого коагулянта при критической концентрации (к. к. к.). Большая часть добавленной соли остается в растворе, поэтому концентрация по существу сохраняется неизменной, в то время как флокуляция развивается. Лишь очень небольшая доля ионов прибавляемой соли адсорбируется на поверхности флокулирую - щих частиц, и потерей этих ионов в самом растворе обычно пренебрегают. В рассматриваемом случае внимание, как правило, в первую очередь концентрируется на свойствах дисперсионной среды, а не на возможной адсорбции ионов на флоку - лирующих частицах.
С другой стороны, когда агентом, вызывающим агрегацию, является полимерная молекула или же другая коллоидная частица, большая доля такого агента адсорбируется на. частицах до тех пор, пока в системе не будет достигнута точка к. к. к., в которой только небольшая часть флокулирующего агента может в действительности находиться в растворе. В таком случае требуемое количество агента непосредственно связывается с поверхностью флокулирующих частиц. Несомненно, имеются также промежуточные ситуации, в частности, когда агент представляет собой многозарядный ион или поликатион небольших размеров.
По-видимому, различие состоит в том, что если флокули - рующим агентом оказывается большая молекула или частица и если этот агент преимущественно адсорбируется на изучаемых частицах, когда в системе имеется критическая концентрация коагулянта, то тогда можно наглядно выявить количество агента, адсорбированного на флокулированных частицах. Однако если такой агент представляет собой простую соль, как, например, хлорид натрия, который требуется в большом избытке в растворе в точке к. к. к., то тогда адсорбцию этого агента на коагулянте не так легко измерить, а также трудно продемонстрировать возможное образование мостиковых связей между частицами посредством ионов соли. Принимается, что вандерваальсовы силы являются источником притяжения частиц; в действительности может происходить удерживание вместе частиц кремнезема в точках их контакта посредством адсорбированных ионов, таких, как Na+.
Вандерваальсовы силы часто называют «дисперсионными силами», что не совсем правильно, так как это силы притяжения, а не дисперсионные в физическом понимании. Роувелер и Овербек исследовали силы, возникающие между кремнеземными поверхностями. Подобным же образом Табор, и Уин - тертон измерили силы между поверхностями пластинок слюды и пришли к заключению, что присутствие воды снижает притяжение примерно в 10 раз.
Вполне вероятно, что дисперсионные силы играют незначительную роль или вовсе не имеют никакого значения в рассматриваемой системе кремнезема. Как отметили Дюмон и Уотиллон , кремнезем представляет собой наиболее сложную из всех известных оксидную систему, так как она проявляет максимальную устойчивость в точке нулевого заряда. В данной точке очень низка константа Гамакера, и поэтому дисперсионные силы оказываются незначительными, так что по крайней мере в некоторых областях значений рН агрегация частиц включает образование химической связи. В более детальном исследовании, выполненном Депассе и Уотиллоном , отмечалось, что одного монослоя воды достаточно, чтобы экранировать дисперсионные силы между небольшими коллоидными частицами кремнезема (меньшими 25 нм в диаметре) .
Таким образом, дисперсионные силы, вероятно, не играют никакой роли, за исключением, может быть, золей с частицами по размеру, большими 100 нм.
Различие между кремнеземом и другими оксидами, согласно - данным Визе и Хили , подчеркивается тем фактом, что оксиды, подобные ТЮ2 и А1203, подвержены флокуляции под действием солей и - величины рН, удовлетворительно объясняемой до известной степени теорией ДЛФО, всякий раз, когда электрокинетический потенциал падает ниже 14 + 4 мВ.
Правила коагуляции электролитами. Порог коагуляции. Правило Шульце-Гарди. Виды коагуляции: концентрационная и нейтрализационная. Коагуляция смесями электролитов. Явление "неправильные ряды". Механизм и кинетика коагуляции
Коагуляцией называется процесс слипания частиц с образованием крупных агрегатов. В результате коагуляции система теряет свою седиментационную устойчивость, так как частицы становятся слишком крупными и не могут участвовать в броуновском движении.
Коагуляция является самопроизвольным процессом, так как она приводит к уменьшению межфазной поверхности и, следовательно, к уменьшению свободной поверхностной энергии.
Различают две стадии коагуляции.
1 стадия – скрытая коагуляция. На этой стадии частицы укрупняются, но еще не теряют своей седиментационной устойчивости.
2 стадия - явная коагуляция. На этой стадии частицы теряют свою седиментационную устойчивость. Если плотность частиц больше плотности дисперсионной среды, образуется осадок.
Причины коагуляции многообразны. Едва ли существует какое либо внешнее воздействие, которое при достаточной интенсивности не вызывало бы коагуляцию.
Правила коагуляции:
1. Все сильные электролиты, добавленные к золю в достаточном количестве, вызывают его коагуляцию.
Минимальная концентрация электролита, при которой начинается коагуляция, называется порогом коагуляции C k .
Иногда вместо порога коагуляции используют величину V K , называемую коагулирующей способностью. Это объем золя, который коагулирует под действием 1 моля электролита:
,т.е. чем меньше порог коагуляции, тем больше коагулирующая способность электролита.
2. Коагулирующим действием обладает не весь электролит, а только тот ион, заряд которого совпадает по знаку с зарядом противоиона мицеллы лиофобного золя. Этот ион называют ионом–коагулянтом .
3. Коагулирующая способность иона–коагулянта тем больше, чем больше заряд иона.
Количественно эта закономерность описывается эмпирическим правилом Щульце – Гарди:
где a - постоянная для данной системы величина;
Z – заряд иона – коагулянта;
- порог коагуляции однозарядного, двухзарядного, трехзарядного иона-коагулянта.Правило устанавливает , что коагулирующие силы иона тем больше, чем больше его валентность . Экспериментально установлено, что ионы с высшей валентностью имеют значение порога коагуляции ниже, чем ионы с низшей. Следовательно, для коагуляции лучше брать ионы с высшей степенью окисления. Если валентность ионов одинакова, то коагулирующая способность зависит от размеров и степени гидратации ионов. Чем больше радиус иона, тем больше его коагулирующая способность. По этому правилу составлены лиотропные ряды . Органические ионы-коагулянты, как правило, лучше коагулируют гидрозоли, чем неорганические, т.к. они легко поляризуются и адсорбируются. С точки зрения двойного электрического слоя (ДЭС) считается, что коагуляция идет в том случае, когда z-потенциал > 30 мВ.
Коагулирующая способность иона при одинаковом заряде тем больше, чем больше его кристаллический радиус . Причина с одной стороны, в большой поляризуемости ионов наибольшего радиуса, следовательно, в их способности притягиваться поверхностью, состоящей из ионов и полярных молекул. С другой стороны, чем больше радиус иона, тем меньше, при одной и той же величине заряда, гидратация иона. Гидратная же оболочка уменьшает электрическое взаимодействие. Коагулирующая способность органических ионов больше по сравнению с неорганическими ионами.
Для однозарядных неорганических катионов коагулирующая способность убывает в следующем порядке:
- лиотропный ряд.При увеличении концентрации иона–коагулянта z – потенциал мицеллы золя уменьшается по абсолютной величине. Коагуляция может начинаться уже тогда, когда z – потенциал снижается до 0,025 – 0, 040 В (а не до нуля).
При коагуляции золя электролитами различают концентрационную и нейтрализационную коагуляцию.
Концентрационная коагуляция имеет место, когда она происходит под действием индифферентного электролита вследствие сжатия диффузного слоя противоионов и уменьшения абсолютного значения z-потенциала.
Рассмотрим концентрационную коагуляцию золя хлорида серебра, стабилизированного нитратом серебра, при введении в золь нитрата калия.
Формула мицеллы имеет вид:
.На рис. 3.1.2.1 показан график изменения потенциала в ДЭС мицеллы хлорида серебра. Кривая 1 относится к исходной мицелле, кривая 2 – после добавления KNO 3 в количестве, вызывающем коагуляцию. При добавлении KNO 3 диффузный слой противоионов сжимается, формула мицеллы приобретает вид:

На рис. 3.1.2.2 представлены потенциальные кривые, характеризующие взаимодействие частиц в этом золе. z-потенциал исходной коллоидной частицы положительный, это создаёт потенциальный барьер коагуляции ∆ U к =0 (кривая 2 рис. 3.1.2.2). Поэтому ничто не мешает коллоидным частицам сблизиться на такое расстояние, где преобладают силы притяжения – происходит коагуляция. Так как в данном случае причиной коагуляции является увеличение концентрации противоионов, она называется концентрационной коагуляцией.
Для этого случая теория дает формулу
где g - порог коагуляции;
С – константа, слабо зависящая от асимметрии электролита, т.е. отношение числа зарядов катиона и аниона;
А – константа;
е – заряд электрона;
e - диэлектрическая проницаемость;
Z – заряд коагулирующего иона;
Т – температура.
Из уравнения следует, что значение порогов коагуляции для одно-, двух-, трех-, четырех- зарядных ионов должны соотноситься 1 к (1/2) 6 к (1/3) 6 к (1/4) 6 и т.д., т.е. обосновывается ранее представленное эмпирическое правило Шульце – Гарди.
Нейтрализационная коагуляция происходит при добавлении к золю неиндифферентного электролита. При этом потенциалопределяющие ионы связываются в малорастворимое соединение, что приводит к уменьшению абсолютных величин термодинамического потенциала, а следовательно, и z-потенциала вплоть до нуля.
Если взять в качестве исходного только что рассмотренный золь хлорида серебра, то для нейтрализации потенциалопределяющих ионов Ag + в золь необходимо ввести, например, хлорид калия. После добавления определённого количества этого неиндифферентного электролита мицелла будет иметь вид:
В системе не будет ионов, способных адсорбироваться на поверхности частицы AgCl , и поверхность станет электронейтральной. При столкновении таких частиц происходит коагуляция.
Так как причиной коагуляции в данном случае является нейтрализация потенциалопределяющих ионов, такую коагуляцию называют нейтрализационной коагуляцией.
Необходимо отметить, что для полной нейтрализационной коагуляции неиндифферентный электролит должен быть добавлен в строго эквивалентном количестве.
При коагуляции смесью электролитов различают два типа процессов:
· гомокоагуляция
· гетерокоагуляция
Гомокоагуляция - укрупнение подобных частиц в больший агрегат осадка. Причем в процессе отстаивания мелкие частицы растворяются, а крупные увеличиваются за их счет. На этом основано явление активации и перекристаллизации. Этот процесс описывается уравнением Кельвина – Томсона:
где С ¥ - растворимость макрочастиц;
С – растворимость микрочастиц;
V м – молярный объем;
R – универсальная газовая постоянная;
T – температура;
r – радиус частиц.
Из уравнения следует, что концентрация вокруг маленького радиуса больше, поэтому диффузия идет от бóльшей концентрации к меньшей.
При втором типе происходит слияние разнородных частиц или прилипание частиц дисперсной системы на вводимые в систему чужеродные тела или поверхности.
Гетерокоагуляция - взаимная коагуляция разнородных дисперсных систем.
Коагуляция смесью электролитов имеет большое практическое значение, так как даже при добавлении к золю одного электролита-коагулянта, в действительности коагуляция происходит, по крайней мере, под влиянием двух электролитов, так как в системе содержится электролит-стабилизатор. Кроме того, в технике для коагуляции часто применяют смесь двух электролитов. Понимание закономерностей взаимного действия электролитов важно также при исследовании воздействия биологически активных ионов на органы и ткани живого организма.

При коагуляции золя смесью двух и более электролитов возможны три случая (рис. 3.1.2.3). По оси абсцисс отложена концентрация первого электролита С 1 , а C к1 – его порог коагуляции. Аналогично по оси ординат отложена концентрация второго электролита С 2 , а С к2 – его порог коагуляции.
Изменение состояния коллоидных систем
Коллоидные системы обладают высокоразвитой поверхностью раздела и, следовательно большим избытком свободной поверхностной энергии. Поэтому эти системы термодинамически неустойчивы. Если в силу создавшихся условий мицеллы золя приходят в тесное соприкосновение между собой, они соединяются в крупные агрегаты.
Коагуляция – это процесс укрепления коллоидных частиц в золях, происходящих под влиянием внешних воздействий
Седиментация – процесс осаждения укрупненных частиц твердой фазы золя.
Процесс коагуляции связан с уменьшением степени дисперсности и обусловлен агрегативной неустойчивостью коллоидных систем.
В коагуляции различают 2 стадии:
1) скрытую коагуляции – когда новорожденным газом еще нельзя наблюдать какие либо внешние изменения в золе.
2) явную коагуляцию, когда процесс агрегации частиц дисперсной фазы золя может быть легко обнаружен визуально.
Коагуляция может быть вызвана повышением температуры, длительным диализом, добавлением электролитов, разного рода механическими воздействиями (размешивание, встряхивание, взбалтывание), сильным охлаждением, ультрацентрифугированием, концентрированием, пропусканием электрического тока, действием на золь другим золем.
Поскольку главное условие уменьшения устойчивости коллоидных растворов – потеря электрического заряда, основными методами их коагулирования являются методы снятия зарядов.
Коагуляция гидрофобных золей электролитами
Чтобы начался процесс коагуляции нужно наличие некоторой минимальной концентрации электролита в золе.
Порог коагуляции – наименьшая концентрация ммоль/л электролита, вызывающая коагуляцию (помутнение раствора, изменение окраски).
Правило Шульце-Гарди – ионы коагуляторы высшей зарядности, вызывают коагуляцию при меньших концентрациях, чем ионы низшей зарядности.
Правило Шульце-Гарди имеет приближенный характер, т.к. коагулирующие действие электролита зависит не только от зарядности его ионов. Некоторые органические однозарядные ионы обладают более сильной адсорбируемостью.
По величине коагулирующей способности ионы щелочных металлов можно расположить в ряды ионов этих металлов – лиотропные ряды.
Cs + >Rb + >NH 4 + >K + >Na + >Li +
Коагуляции гидрофобных золей можно вызвать при помощи смеси электролитов. При этом возможны 3 случая:
1)Коагулирующие действие смешиваемых электролитов суммируется.
2)Коагулирующие действие смеси электролитов меньше, чем в случае чистых электролитов. Это явление носит название антогонизма ионов. Оно характерно для смесей ионов, имеющих различную валентность.
3)В ряде случаев имеет место взаимное усиление коагулирующего действия смешиваемых ионов. Это явление называется синергизмом ионов.
Коагуляция гидрофобных коллоидов может быть вызвана смешиванием в определенных количественных соотношениях с другим гидрофобным золем, гранулы которого имеют противоположный знак. Это явление называется взаимной коагуляцией . Взаимная коагуляция происходит при смешивании морской и речной воды. При этом ионы солей морской воды адсорбируются на заряженных коллоидных частицах речной воды, в результате чего происходит их коагуляция. По этой причине на дне постоянно скапливается большое количество ила, образуется много мелей и островков.
В быту: чернила представляют собой коллоидные растворы различных красителей. Причем в разных чернилах коллоидные частицы заряжены по-разному. Вот почему при смешивании разных чернил имеет место взаимная коагуляция.
Механизм электролитной коагуляции
Гранула становится электронейтральной в том случае, если противоионы диффузного слоя, заряженные отрицательно, перемещаются в адсорбционный слой. Чем выше концентрация прибавляемого электролита, тем сильнее снижается диффузный слой, тем меньше становится потенциал, тем быстрее начинается процесс коагуляции. При определенной концентрации электролита практически все противоионы перейдут в адсорбированный слой, заряд гранулы снизится до нуля и коагуляция пойдет с максимальной скоростью.
Коагулирующее действие электролитов сводится к сжатию диффузного слоя и протекает избирательная адсорбция на коллоидной частице тех ионов электролитов, которые имеют заряд, противоположный грануле. Чем выше заряд иона, тем интенсивнее он адсорбируется. Накопление ионов в адсорбированном слое сопровождается уменьшением потенциала и диффузного слоя.
Вывод: коагулирующие действие электролитов заключается в уменьшении сил отталкивания между коллоидными частицами через понижение потенциала и изменение строение двойного электрического слоя и сжатия диффузной его части, обусловленное прибавлением электролита – коагулянта, влечет за собой понижение расклинивающего действия гидратных оболочек диффузных ионов, разъединяющих коллоидные частицы.
При добавлении к золям электролитов с многозарядными ионами, заряд которых противоположен по знаку заряду коллоидных частиц, может наблюдаться не коагуляция, а стабилизация золя и перемена потенциала. Это явление называется перезарядка золей.
Способность дисперсных систем сохранять определенную степень дисперсности называется агрегативной устойчивостью.
Частицы дисперсной фазы сопротивляются слипанию за счет разных механизмов. Данная способность обусловлена во-первых образованием на поверхности частиц дисперсной фазы двойного электрического слоя,обеспечивающего электрическую стабилизацию дисперсной системы.Во-вторых, работаетмолекулярно-адсорбционный механизм стабилизации, заключающийся в образовании вокруг частиц слоёв адсорбции, состоящих из молекул дисперсной среды и растворённых в ней веществ. В-третьих, существует кинетический фактор устойчивости - малая частота столкновений дисперсных частиц.
Золи (коллоидные растворы) отличаются от грубодисперсных и молекулярных систем агрегативной неустойчивостью, поэтому они меняются как во времени, так и при добавках различных веществ.
Суть механизма очистки воды от взвешенных коллоидных частицсостоит в нарушении равновесного состояния системы - устранения баланса сил, не позволяющихчастицам осесть.
Для достижения этой цели использует процесс коагуляции коллоидных примесей (упрощённо - коагуляция воды).
Коагуляция - процесс слипания коллоидов в более крупные агрегаты, происходящее в результате их столкновенийприброуновском движении, смешении или направленном перемещении во внешнем силовом поле, добавлении коагулянтов. При этом происходит выпадение осадка - коагулята.
Коагулянты (обычно это растворимые соли железа или алюминия) интенсифицируютпроцесс коагуляции. Введение в воду этих веществ способствует образованию новой малорастворимой фазы (в результате гидролиза - взаимодействия вещества с водой). Таким образом, процесскоагуляции заключается в прогрессирующем укрупнении частиц и уменьшении их численности в объёме дисперсионной среды.
Коагуляция бывает медленная и быстрая. При медленной коагуляции только незначительная часть соударений частиц-коллоидов приводит их к слипанию, а коагулят не выпадает. При быстрой коагуляции каждое соударение обладает эффективностьюи влечёт слипание частиц, а в коллоидном растворе постепенно образуется осадок.
Минимальную концентрацию дозируемого вещества (электролита или не электролита), инициирующего процесс коагуляции в системе с жидкой дисперсионной средой, называют порогом коагуляции. При определенных условиях коагуляция обратима. Процесс перехода коагулята обратно в золь называютпептизацией, а провоцирующие этот процессвещества - пептизаторами. Пептизаторы, являясь стабилизаторами дисперсных систем, адсорбируются на поверхностичастиц, ослабляя взаимодействие между ними, в результате чего происходит распад агрегатов. Особенно эффективно возврат в первичное состояние проходитпри вводе в среду поверхностно-активных веществ, снижающих поверхностную межфазную энергию и облегчающих диспергирование.
Коагуляция с применением солей железа
Рассмотрим, какие процессы протекают при добавлении в коллоидный раствор сульфата железа (III). Этот коагулянт в водном растворе диссоциирует на ионы железа и сульфат-ион :
Fe 2 (SO 4) 3 → 2 Fe 3+ + 3 SO 4 2-
Fe 3+ + H 2 O ↔ Fe(OH) 2+ + H +
Fe(OH) 2+ + H 2 O ↔ Fe(OH) 2 + + H +
Fe(OH) 2 + + H 2 O ↔ Fe(OH) 3 ↓ + H +
Fe 3+ + 3H 2 O ↔ Fe(OH) 3 ↓ + 3H +
Мицелла - структурная единица лиофобных (слабо взаимодействующих с жидкостью) коллоидов, не имеющая определенного состава. Схематически ее строение на примере мицеллы гидроксида железа (III) может быть изображено схемой:
{mFe(OH) 3 2nFe(OH) 2+ (2n - x) SO 4 2- }2x+ xSO 4 2-
 Микрокристалл гидроксида железа,образующий коллоидную частицу (см. рисунок), избирательно адсорбирует из окружающей среды ионы, идентичные ионам его кристаллической решетки. В зависимости от химического состава раствора (избыток сульфат - ионов илиизбыток ионов железа) микрокристаллприобретает отрицательный или положительный заряд. Такой заряженный кристалл называется ядром мицеллы, а сообщают ему этот заряд потенциалопределяющие ионы.
Микрокристалл гидроксида железа,образующий коллоидную частицу (см. рисунок), избирательно адсорбирует из окружающей среды ионы, идентичные ионам его кристаллической решетки. В зависимости от химического состава раствора (избыток сульфат - ионов илиизбыток ионов железа) микрокристаллприобретает отрицательный или положительный заряд. Такой заряженный кристалл называется ядром мицеллы, а сообщают ему этот заряд потенциалопределяющие ионы.
Электрическое поле заряженной поверхности кристалла притягивает из раствора противоионы - ионы, несущие противоположный заряд. На границе раздела фаз образуется двойной электрический слой, толщину которого определяет внешняя граница облака противоионов.
Двойной электрический слой состоит из адсорбционой и диффузной частей. Адсорбционный слой включает в себя потенциалобразующие ионы и часть противоионов, адсорбированных на поверхности ядра. Диффузный слой достраивают остальные противоионы в количестве, способствующем электронейтральности мицеллы.
Двойной электрический слой, окружающий коллоиды, под воздействием коагулянтов (электролитов), перестраивается: противоионы начинают вытесняться из диффузной в адсорбционную часть, и толщина всего электрического слоя со временем уменьшается до толщины адсорбционного слоя. Дисперсные частицы попадают в область взаимного притяжения, инаступает быстрая коагуляция.
Коагуляция с применением солей алюминия
 Чаще всего для очистки воды коагуляцией на отечественных станциях водоподготовки и вбассейнах используют 18-ти водный кристаллогидрат сульфата алюминия - Al 2 (SO 4) 3 . 18 H 2 O.
Чаще всего для очистки воды коагуляцией на отечественных станциях водоподготовки и вбассейнах используют 18-ти водный кристаллогидрат сульфата алюминия - Al 2 (SO 4) 3 . 18 H 2 O.
Процессы, протекающие при введении в воду солей алюминия, аналогичны вышеописанным при добавлении солей железа:
Al 3+ + H 2 O ↔ Al(OH) 2+ + H +
Al(OH) 2+ + H 2 O ↔ Al(OH) 2 + + H +
Al(OH) 2 + + H 2 O ↔ Al(OH) 3 ↓ + H +
Суммарное уравнение гидролиза:
Al 3+ + 3H 2 O ↔ Al(OH) 3 ↓ + 3H +
Образование осадка гидроксида алюминия происходит при значениях рН в диапазонеот 5 до 7,5. При рН < 5 осадок не образуется. При рН > 8,5 идет растворение образованного гидроксида алюминия с образованием алюминатов.
Al 2 (SO 4) 3 + 6 NaOH = 2 Al(OH) 3 ↓ + 3 Na 2 SO 4
Al(OH) 3 + NaOH = Na или (NaAlO 2 . 2H 2 O)
Современные коагулянты
Все большее распространение в процессах водоподготовкии очистки сточных вод получаюткоагулянты на основе полиоксихлорида алюминия.
Преимущества этих коагулянтов по сравнению с сульфатом алюминия:
Поставка в виде растворов, что делает более удобным их применение (не надо растворять);
Большее процентное содержание активного вещества;
Получение очищенной воды более высокого качества;
Сокращение объёма вторичных отходов;
Низкое остаточноесодержание алюминия (< 0,2 мг/л);
Не требуется корректировать рН;
Широкий диапазон рабочих температур.
Технические характеристики таких коагулянтов производства ОАО «АУРАТ»:

Контактная коагуляция
 Один из вариантов очистки методом коагуляции - контактная коагуляция. Контактная коагуляцияпроисходит на зёрнах загрузки напорных вертикальных фильтров механической очистки. При этом введение коагулянта осуществляется непосредственно перед механическим фильтром. Зерна загрузки и частицы, адсорбированные на них, служат центрами коагуляции. Процесс хлопьеобразования в этом случае значительно ускоряется.
Один из вариантов очистки методом коагуляции - контактная коагуляция. Контактная коагуляцияпроисходит на зёрнах загрузки напорных вертикальных фильтров механической очистки. При этом введение коагулянта осуществляется непосредственно перед механическим фильтром. Зерна загрузки и частицы, адсорбированные на них, служат центрами коагуляции. Процесс хлопьеобразования в этом случае значительно ускоряется.
Протекание процесса коагуляции с более высокой скоростью и отсутствие необходимости в отстойниках для формирования и осаждения хлопьев осадка являются несомненными преимуществами контактной коагуляции.
К недостаткам контактной коагуляции относится ускоренное загрязнение напорных фильтров и потребность в частой регенерации загрузки, а также опасность проскока реагента в случае неправильного подбора режима коагуляции/фильтрования.
Чтобы проверить - осуществляется ли контактная коагуляция или нет, воду после механических фильтров проверяют на содержание коагулянта.
Уважаемые господа, если у Вас имеется потребность реализации очистки воды с помощью коагулянтов для доведения качества воды до определённых нормативов, сделайте запрос специалистам компании Waterman . Мы разработаем для Вас оптимальную технологическую схему очистки воды.