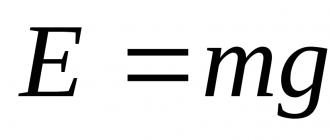Трансляция
(от лат. translatio
— перевод) — термин, обозначающий в биологии такие реакции, в результате которых в рибосомах с использованием в качестве матрицы иРНК осуществляется синтез полипептидной цепи.
В процессе синтеза полипептидная цепь удлиняется в результате последовательного присоединения отдельных аминокислотных остатков. Для того чтобы понять, каким образом осуществляется образование пептидной связи между соответствующими аминокислотами, необходимо рассмотреть структуру рибосом и транспортных РНК (тРНК), участвующих с процессе трансляции.
В состав каждой рибосомы входят 2 субъединицы: большая и малая, которые могут отделяться друг от друга. В состав каждой из этих субъединиц входят рибосомная РНК и белок. Некоторые рибосомные белки являются ферментами, т.е. выполняют каталитические функции. Главная функция малой субъединицы — «расшифровка» генетической информации. Она связывает иРНК и тРНК, несущие аминокислоты. Функция большой субъединицы — образование пептидной связи между аминокислотами, которые принесены в рибосому двумя соседними молекулами тРНК.
Транспортная РНК.
Молекулы транспортных РНК невелики, в их состав входят 70-90 нуклеотидов. Функция тРНК заключается в том, чтобы в ходе процесса синтеза полипептидной цепи переносить на рибосомы определенные аминокислоты, при этом каждая аминокислота переносится соответствующей тРНК. Все молекулы тРНК могут образовывать характерную конформацию (пространственное расположение атомов в молекуле) — конформацию клеверного листа. Такая конформация молекулы тРНК возникает потому, что в ее структуре имеется значительное количество нуклеотидов (по 4-7 в одном участке), комплементарных друг другу. Внутримолекулярное спаривание таких нуклеотидов за счет образования водородных связей между комплементарными основаниями и приводит к образованию такой структуры. В вершине клеверного листа расположен триплет нуклеотидов, который комплементарен кодону иРНК, кодирующему аминокислоту. Этот триплет отличается у тРНК, переносящих различные аминокислоты, он кодирует определенную аминокислоту, именно ту, которую переносит данная тРНК. Его называют антикодоном .
Антикодон молекулы тРНК и кодон молекулы иРНК
В основании клеверного листа есть участок, в котором связывается аминокислота. Таким образом, получается, что молекула тРНК не только переносит определенную аминокислоту, в ее структуре есть запись о том, что она переносит именно данную аминокислоту, причем эта запись сделана на языке генетического кода.
Как уже говорилось, рибосомы способны связывать иРНК, несущую информацию об аминокислотной последовательности синтезируемого белка, тРНК, несущие аминокислоты, и, наконец, синтезируемую полипептидную цепь. Малая субъединица рибосомы связывает иРНК и тРНК, несущую первую аминокислоту полипептидной цепи (обычно это метионин), после чего происходит связывание большой субъединицы с образованием функционирующей (работающей) рибосомы. Активный центр рибосомы, где образуется пептидная связь между двумя соседними аминокислотами, устроен так, что в нем могут одновременно находиться два соседних кодона (триплета) иРНК. На первом этапе за счет взаимодействия между кодоном и антикодоном происходит связывание тРНК с иРНК. Т.к. антикодон, находящийся на тРНК, и кодон, расположенный на иРНК, комплементарны, между входящими в их состав азотистыми основаниями образуются водородные связи. На втором этапе аналогичным образом осуществляется связывание с соседним кодоном второй молекулы тРНК. Молекулы тРНК в активном центре рибосомы на этом этапе располагаются таким образом, что группа -С=О первого аминокислотного остатка, который связан с первой тРНК, оказывается вблизи от свободной аминогруппы (-NH 2) аминокислотного остатка, входящего в состав второй транспортной тРНК. Таким образом, благодаря взаимодействию кодон-антикодон между последовательно расположенными кодонами иРНК и соответствующими им антикодонами тРНК рядом располагаются именно те аминокислоты, которые последовательно закодированы в иРНК.

Активный центр рибосомы, в котором осуществляется образование пептидной связи между двумя соседними аминокислотами
На следующем этапе при взаимодействии свободной аминогруппы, входящей в состав аминокислотного остатка вновь пришедшей тРНК, с карбоксильной группой аминокислотного остатка первой аминокислоты, между двумя аминокислотами, прикрепленными к соответствующим тРНК, образуется пептидная связь. Реакция осуществляется путем замещения, при этом уходящей группой является молекула первой тРНК. В результате такого замещения удлинившаяся тРНК, несущая уже дипептид, оказывается связанной с рибосомой. Для прохождения данной реакции необходим фермент, который есть в составе большой субъединицы рибосомы.
На последнем этапе пептид, связанный с второй молекулой тРНК, передвигается с участка, в котором в начале цикла была связана тРНК, содержащая аминокислоту, в участок, где связывается тРНК с образующимся пептидом. Одновременно с перемещением синтезирующейся пептидной цепи происходит перемещение рибосомы вдоль иРНК, при этом в ее (рибосомы) активном центре оказывается следующий кодон иРНК, после этого события, описанные выше, повторяются. Синтез белка осуществляется с очень большой скоростью, пептид, состоящий из 100 аминокислот, синтезируется примерно за 1 минуту.
Рибосома продвигается вдоль нитевидной молекулы иРНК по мере того, как происходит сборка полипептидной цепи. На одной молекуле иРНК может одновременно находиться несколько рибосом, и каждая из них осуществляет синтез полипептидной цепи, закодированной этой тРНК, в результате чего формируются полисомы : рибосомы, нанизанные на нить иРНК. Чем дальше рибосома проходит по цепи иРНК, тем более длинный фрагмент молекулы белка будет синтезирован. Синтез белка заканчивается, когда рибосома достигнет конца молекулы иРНК, после этого рибосома с вновь синтезированным белком покидает молекулу иРНК (см. рисунок ниже). Сигнал о том, что синтез полипептидной цепи закончен, подается тремя специальными кодонами, один из которых присутствует в терминальной части молекулы иРНК. Считывание информации с молекулы иРНК возможно только в одном направлении.

Процесс синтеза белка
Только что образованный конец полипептидной цепи еще во время синтеза может связываться со специальными белками шаперонами , которые обеспечат ее правильную укладку, а затем направляется к аппарату Гольджи, откуда белок транспортируется в то место, где он будет работать. Рибосома, которая освободилась от иРНК и синтезированной полипептидной цепи, распадается на субъединицы, после чего большая субъединица, снова может связаться с малой и образовать активную рибосому, способную синтезировать новый (или тот же самый) белок.
Как я рассказывал ранее, любые процессы синтеза, в результате которых из более простых молекул образуются более сложные, осуществляются с затратой энергии. Биосинтез белка — это целая цепь реакций, протекающих с затратой энергии. Так, например, для связывания одной аминокислоты с тРНК необходима энергия двух макроэргических связей молекулы АТФ. Кроме того, при образовании одной пептидной связи используется энергия еще одной макроэргической связи. Таким образом, при образовании одной пептидной связи в молекуле белка затрачивается количество энергии, запасенное в трех макроэргических связях молекул АТФ.
В молекуле белка различают прочные, ковалентные связи: пептидные, дисульфидные и непрочные, нековалентные связи: водородные, ионные, вандерваальсовые, гидрофобные.
Пептидные связи
Пептидные связи (-СО-NН-) являются основным видом связей в белках. Впервые они были изучены А.Я. Данилевским (1888 г.). Пептидные связи образуются при взаимодействии α- карбоксильной группы одной аминокислоты и α - аминогруппой другой аминокислоты. Пептидная связь является сопряжённой связью, электронная плотность в ней смещена от азота к кислороду, в силу чего она занимает промежуточное положение между одинарной и двойной связью. Длина пептидной связи составляет 0,132 нм. Вращение атомов вокруг пептидной связи затруднено, атомы О и Н в ней находятся в транс-положении. Все атомы пептидной связи располагаются в одной плоскости. Атомы О и Н пептидной связи могут дополнительно образовывать водородные связи с другой пептидной связью. Пептидные связи определяют порядок чередования аминокислот в полипептидной цепи белка, т.е. формируют первичную структуру белка. Пептидные связи – прочные связи (энергия разрыва составляет около 95 ккал/моль). Расщепление пептидных связей осуществляется при кипячении белка в присутствии кислот, щелочей или под действием ферментов пептидаз.
Дисульфидные связи
Дисульфидные связи (-S- S-) образованы двумя молекулами цистеина в составе белковой молекулы. Возможны внутрицепочечные дисульфидные «мостики» в пределах одной полипептидной цепи и межцепочечные связи между отдельными полипептидными цепями. Например, в молекуле гормона инсулина присутствуют оба варианта дисульфидных связей. Дисульфидные связи влияют на пространственную укладку белковой молекулы, т.е. на третичную структуру белков. Дисульфидные связи разрываются при действии некоторых восстановителей и при денатурации белка.
Водородные связи
Водородные связивозникают между атомом водорода и электроотрицательным атомом (чаще кислородом). Водородные связи примерно в 10 раз слабее пептидных связей. Наиболее часто они возникают между атомом Н и атомом О различных пептидных связей: либо близко расположенных в молекуле белка, либо находящихся в разных полипептидных цепях. Большое количество водородных связей фиксирует в белках в основном вторичную структуру (α - спираль и β - складчатую структуру) а также участвует в образовании третичной и четвертичной структур белка. Непрочные водородные связи легко разрываются при денатурации белка.
Ионные связи
Ионные связи образуются между противоположно заряженными аминокислотами в составе белковой молекулы (положительно заряженными лизином, аргинином, гистидином и отрицательно заряженными глютаматом и аспартатом). Ионные связи влияют на пространственную укладку белков, т.е. формируют третичную и четвертичную структуры белков. Ионные связи нарушаются при изменении рН среды, при денатурации.
Вандерваальсовые взаимодействия
Вандерваальсовые взаимодействия – разновидность связей, возникающих при кратковременной поляризации атомов.
Гидрофобные связи
Гидрофобные связи возникают между неполярными (гидрофобными) радикалами аминокислот в полярном растворителе (вода). Гидрофобные радикалы погружаются внутрь белковой молекулы, меняя пространственное расположение полипептидной цепи. Гидрофобные взаимодействия имеют энтропийную природу, придают устойчивость молекуле белка, участвуя в формировании его третичной, а также четвертичной структуры.
Ионная связь аминокислот. Дисульфидная связь аминокислот. Водородная связь аминокислот.
При определенных значениях рН кислотные и основные R-группы ионизованы, т. е. несут заряд, кислотные - отрицательный, а основные - положительный. Благодаря этому они могут взаимодействовать друг с другом, в результате чего возникает ионная связь.
В водной среде ионные связи значительно слабее ковалентных и могут разрываться при изменении рН среды. Это объясняет, почему при изменении рН может разрушаться структура белка .
Если, например, к молоку добавить кислоту, то молоко свернется: казеин (белок молока) из-за разрыва ионных связей станет нерастворимым.
Дисульфидная связь аминокислот
Молекула аминокислоты цистеина содержит сульфгидрильную (-SH) группу. Когда соединяются две молекулы цистеина, их сульфгидрильные группы, оказавшись по соседству, окисляются и образуют дисульфидную связь .
Дисульфидные связи могут возникать как между разными полипептидными цепями (в молекуле инсулина), так и между различными участками одной и той же полипептидной цепи . В последнем случае именно они вынуждают молекулу определенным образом свертываться, т. е. приобретать свойственную ей форму.
Дисульфидные связи достаточно прочны и разрываются нелегко.

Водородная связь аминокислот
О водородной связи мы уже говорили выше при обсуждении свойств воды. Когда водород входит в состав ОН- или NH-группы, он несет небольшой положительный заряд.
Объясняется это тем, что обобщенные электроны, заряженные отрицательно, притягиваются атомами О или N сильнее, чем водорода . Водород будет поэтому притягиваться оказавшимися с ним по соседству атомами кислорода С=0-групп или атомами азота NH-групп. С=0- и NH-группы регулярно чередуются вдоль полипептидной цепи, поэтому такие взаимодействия ведут к появлению структур, подобных а-спирали, о которой мы будем говорить ниже.
Водородные связи слабы, но они возникают очень часто, так что общий их вклад в стабильность молекулярной структуры, например в структуру альфа-спирали или белка шелка, весьма значителен.
Типы связей между аминокислотами в молекуле белка
1. Ковалентные связи - обычные прочные химические связи.
а) пептидная связь
б) дисульфидная связь
2. Нековалентные (слабые) типы связей - физико-химические взаимодействия родственных структур. В десятки раз слабее обычной химической связи. Очень чувствительны к физико-химическим условиям среды. Они неспецифичны, то есть соединяются друг с другом не строго определенные химические группировки, а самые разнообразные химические группы, но отвечающие определенным требованиям.
а) Водородная связь
б) Ионная связь
в) Гидрофобное взаимодействие
ПЕПТИДНАЯ СВЯЗЬ.
Формируется за счет COOH-группы одной аминокислоты и NH 2 -группы соседней аминокислоты. В названии пептида окончания названий всех аминокислот, кроме последней, находящейся на «С»-конце молекулы меняются на «ил»
Тетрапептид: валил-аспарагил-лизил-серин
 |
Пептидная связь формируется только за счет альфа-аминогруппы и соседней cooh-группы общего для всех аминокислот фрагмента молекулы! Если карбоксильные и аминогруппы входят в состав радикала, то они никогда не участвуют в формировании пептидной связи в молекуле белка.
Любой белок - это длинная неразветвленная полипептидная цепь, содержащая десятки, сотни, а иногда более тысячи аминокислотных остатков. Но какой бы длины ни была полипептидная цепь, всегда в основе ее - стержень молекулы, абсолютно одинаковый у всех белков. Каждая полипептидная цепь имеет N-конец, на котором находится свободная концевая аминогруппа и С-конец, образованный концевой свободной карбоксильной группой. На этом стержне сидят как боковые веточки радикалы аминокислот. Числом, соотношением и чередованием этих радикалов один белок отличается от другого. Сама пептидная связь является частично двойной в силу лактим-лактамной таутомерии. Поэтому вокруг нее невозможно вращение, а сама она по прочности в полтора раза превосходит обычную ковалентную связь. На рисунке видно, что из каждых трех ковалентных связей в стержне молекулы пептида или белка две являются простыми и допускают вращение, поэтому стержень (вся полипептидная цепь) может изгибаться в пространстве.
Хотя пептидная связь довольно прочная, ее сравнительно легко можно разрушить химическим путем – кипячением белка в крепком растворе кислоты или щелочи в течении 1-3 суток.
К ковалентным связям в молекуле белка помимо пептидной, относится также дисульфидная связь .
Цистеин - аминокислота, которая в радикале имеет SH-группу, за счет которой и образуются дисульфидные связи.
 |
Дисульфидная связь - это ковалентная связь. Однако биологически она гораздо менее устойчива, чем пептидная связь. Это объясняется тем, что в организме интенсивно протекают окислительно-восстановительные процессы. Дисульфидная связь может возникать между разными участками одной и той же полипептидной цепи, тогда она удерживает эту цепь в изогнутом состоянии. Если дисульфидная связь возникает между двумя полипептидами, то она объединяет их в одну молекулу.
Слабые типы связейВ десятки раз слабее ковалентных связей. Это не определенные типы связей, а неспецифическое взаимодействие, которое возникает между разными химическими группировками, имеющими высокое сродство друг к другу (сродство – это способность к взаимодействию). Например: противоположно заряженные радикалы.
Таким образом, слабые типы связей - это физико-химические взаимодействия. Поэтому они очень чувствительны к изменениям условий среды (температуры, pH среды, ионной силы раствора и так далее).
Водородная связь - это связь, возникающая между двумя электроотрицательными атомами за счет атома водорода, который соединен с одним из электроотрицательных атомов ковалентно (см. рисунок).
 |
Водородная связь примерно в 10 раз слабее, чем ковалентная. Если водородные связи повторяются многократно, то они удерживают полипептидные цепочки с высокой прочностью. Водородные связи очень чувствительны к условиям внешней среды и присутствию в ней веществ, которые сами способны образовывать такие связи (например, мочевина).
Ионная связь - возникает между положительно и отрицательно заряженными группировками (дополнительные карбоксильные и аминогруппы), которые встречаются в радикалах лизина, аргинина, гистидина, аспарагиновой и глутаминовой кислот.
 |
Гидрофобное взаимодействие - неспецифическое притяжение, возникающее в молекуле белка между радикалами гидрофобных аминокислот - вызывается силами Ван-дер-Ваальса и дополняется выталкивающей силой воды. Гидрофобное взаимодействие ослабевает или разрывается в присутствии различных органических растворителей и некоторых детергентов. Например, некоторые последствия действия этилового спирта при проникновении его внутрь организма обусловлены тем, что под его влиянием ослабляются гидрофобные взаимодействия в молекулах белков.
Пространственная организация белковой молекулы
В основе каждого белка лежит полипептидная цепь. Она не просто вытянута в пространстве, а организована в трехмерную структуру. Поэтому существует понятие о 4-х уровнях пространственной организации белка, а именно - первичной, вторичной, третичной и четвертичной структурах белковых молекул.
ПЕРВИЧНАЯ СТРУКТУРАПервичная структура белка - последовательность аминокислотных фрагментов, прочно (и в течение всего периода существования белка) соединенных пептидными связями. Существует период полужизни белковых молекул - для большинства белков около 2-х недель. Если произошел разрыв хотя бы одной пептидной связи, то образуется уже другой белок.
ВТОРИЧНАЯ СТРУКТУРАВторичная структура - это пространственная организация стержня полипептидной цепи. Существуют 3 главнейших типа вторичной структуры:
1) Альфа-спираль - имеет определенные характеристики: ширину, расстояние между двумя витками спирали. Для белков характерна правозакрученная спираль. В этой спирали на 10 витков приходится 36 аминокислотных остатков. У всех пептидов, уложенных в такую спираль, эта спираль абсолютно одинакова. Фиксируется альфа-спираль с помощью водородных связей между NH-группами одного витка спирали и С=О группами соседнего витка. Эти водородные связи расположены параллельно оси спирали и многократно повторяются, поэтому прочно удерживают спиралеобразную структуру. Более того, удерживают в несколько напряженном состоянии (как сжатую пружину).


Бета-складчатая структура - или структура складчатого листа. Фиксируется также водородными связями между С=О и NH-группами. Фиксирует два участка полипептидной цепи. Эти цепи могут быть параллельны или антипараллельны. Если такие связи образуются в пределах одного пептида, то они всегда антипараллельны, а если между разными полипептидами, то параллельны.
3) Нерегулярная структура - тип вторичной структуры, в котором расположение различных участков полипептидной цепи относительно друг друга не имеет регулярного (постоянного) характера, поэтому нерегулярные структуры могут иметь различную конформацию.
ТРЕТИЧНАЯ СТРУКТУРАЭто трехмерная архитектура полипептидной цепи – особое взаимное расположение в пространстве спиралеобразных, складчатых и нерегулярных участков полипептидной цепи. У разных белков третичной структуры различна. В формировании третичной структуры участвуют дисульфидные связи и все слабые типы связей.
Выделяют два общих типа третичной структуры:
1) В фибриллярных белках (например, коллаген, эластин) молекулы которых имеют вытянутую форму и обычно формируют волокнистые структуры тканей, третичная структура представлена либо тройной альфа-спиралью (например, в коллагене), либо бета-складчатыми структурами.
2) В глобулярных белках, молекулы которых имеют форму шара или эллипса (латинское название: GLOBULA - шар), встречается сочетание всех трех типов структур: всегда есть нерегулярные участки, есть бета-складчатые структуры и альфа-спирали.
Обычно в глобулярных белках гидрофобные участки молекулы находятся в глубине молекулы. Соединяясь между собой, гидрофобные радикалы образуют гидрофобные кластеры (центры). Формирование гидрофобного кластера вынуждает молекулу соответствующим образом изгибаться в пространстве. Обычно в молекуле глобулярного белка бывает несколько гидрофобных кластеров в глубине молекулы. Это является проявлением двойственности свойств белковой молекулы: на поверхности молекулы - гидрофильные группировки, поэтому молекула в целом - гидрофильная, а в глубине молекулы - спрятаны гидрофобные радикалы.
ЧЕТВЕРТИЧНАЯ СТРУКТУРАВстречается не у всех белков, а только у тех, которые состоят из двух или более полипептидных цепей. Каждая такая цепь называется субъединицей данной молекулы (или протомером). Поэтому белки, обладающие четвертичной структурой, называют олигомерными белками. В состав белковой молекулы могут входить одинаковые или разные субъединицы. Например, молекула гемоглобина «А» состоит из двух субъединиц одного типа и двух субъединиц другого типа, то есть является тетрамером. Фиксируются четвертичные структуры белков всеми типами слабых связей, а иногда еще и дисульфидными связями.
КОНФИГУРАЦИЯ И КОНФОРМАЦИЯ БЕЛКОВОЙ МОЛЕКУЛЫИз всего сказанного можно заключить, что пространственная организация белков очень сложна. В химии существует понятие - пространственная конфигурация - жестко закрепленное ковалентными связями пространственное взаимное расположение частей молекулы (например: принадлежность к L-ряду стереоизомеров или к D-ряду).
Для белков также используется понятие конформация белковой молекулы - определенное, но не застывшее, не неизменное взаимное расположение частей молекулы. Так как конформация белковой молекулы формируется при участии слабых типов связей, то она является подвижной (способной к изменениям), и белок может изменять свою структуру. В зависимости от условий внешней среды молекула может существовать в разных конформационных состояниях, которые легко переходят друг в друга. Энергетически выгодными для реальных условий являются только одно или несколько конформационных состояний, между которыми существует равновесие. Переходы из одного конформационного состояния в другое обеспечивают функционирование белковой молекулы. Это обратимые конформационные изменения (встречаются в организме, например, при проведении нервного импульса, при переносе кислорода гемоглобином). При изменении конформации часть слабых связей разрушается, и образуются новые связи слабого типа.
ЛИГАНДЫВзаимодействие белка с каким-нибудь веществом иногда приводит к связыванию молекулы этого вещества молекулой белка. Этот явление известно как «сорбция» (связывание). Обратный же процесс - освобождение другой молекулы от белковой называется «десорбция».
Если для какой-нибудь пары молекул процесс сорбции преобладает над десорбцией, то это уже специфическая сорбция, а вещество, которое сорбируется, называется «лиганд».
Виды лигандов:
1) Лиганд белка-фермента – субстрат.
2) Лиганд траспортного белка – транспортируемое вещество.
3) Лиганд антитела (иммуноглобулина) – антиген.
4) Лиганд рецептора гормона или нейромедиатора – гормон или нейромедиатор.
Белок может изменять свою конформацию не только при взаимодействии с лигандом, но и в результате любого химического взаимодействия. Примером такого взаимодействия может служить присоединение остатка фосфорной кислоты.
В природных условиях белки имеют несколько термодинамически выгодных конформационных состояний. Это нативные состояния (природные). Natura (лат.) – природа.
НАТИВНОСТЬ БЕЛКОВОЙ МОЛЕКУЛЫНативность - это уникальный комплекс физических, физико-химических, химических и биологических свойств белковой молекулы, который принадлежит ей, когда молекула белка находится в естественном, природном (нативном) состоянии.
Например: белок хрусталика глаза - кристаллин - обладает высокой прозрачностью только в нативном состоянии).
ДЕНАТУРАЦИЯ БЕЛКАДля обозначения процесса, при котором нативные свойства белка теряются, используют термин денатурация.
Денатурация - это лишение белка его природных, нативных свойств, сопровождающееся разрушением четвертичной (если она была), третичной, а иногда и вторичной структуры белковой молекулы, которое возникает при разрушении дисульфидных и слабых типов связей, участвующих в образовании этих структур. Первичная структура при этом сохраняется, потому что она сформирована прочными ковалентными связями. Разрушение первичной структуры может произойти только в результате гидролиза белковой молекулы длительным кипячением в растворе кислоты или щелочи.
ФАКТОРЫ, ВЫЗЫВАЮЩИЕ ДЕНАТУРАЦИЮ БЕЛКОВФакторы, которые вызывают денатурацию белков, можно разделить на физические и химические.
Физические факторы
1. Высокие температуры. Для разных белков характерна различная чувствительность к тепловому воздействию. Часть белков подвергается денатурации уже при 40-50°С. Такие белки называют термолабильными . Другие белки денатурируют при гораздо более высоких температурах, они являются термостабильными .
2. Ультрафиолетовое облучение
3. Рентгеновское и радиоактивное облучение
4. Ультразвук
5. Механическое воздействие (например, вибрация).
Химические факторы
1. Концентрированные кислоты и щелочи. Например, трихлоруксусная кислота (органическая), азотная кислота (неорганическая).
2. Соли тяжелых металлов (например, CuSO 4).
3. Органические растворители (этиловый спирт, ацетон)
4. Растительные алкалоиды.
5. Мочевина в высоких концентрациях
 |
5. Другие вещества, способные нарушать слабые типы связей в молекулах белков.
Воздействие факторами денатурации применяют для стерилизации оборудования и инструментов, а также как антисептики.
Обратимость денатурацииВ пробирке (in vitro) чаще всего это – необратимый процесс. Если же денатурированный белок поместить в условия, близкие к нативным, то он может ренатурировать, но очень медленно, и такое явление характерно не для всех белков.
In vivo, в организме, возможна быстрая ренатурация. Это связано с выработкой в живом организме специфических белков, которые «узнают» структуру денатурированного белка, присоединяются к нему с помощью слабых типов связи и создают оптимальные условия для ренатурации. Такие специфические белки известны как «белки теплового шока» или «белки стресса».
Белки стрессаСуществует несколько семейств этих белков, они отличаются по молекулярной массе.
Например, известен белок hsp 70 – heatshock protein массой 70 kDa.
Такие белки есть во всех клетках организма. Они выполняют также функцию транспорта полипептидных цепей через биологические мембраны и участвуют в формировании третичной и четвертичной структур белковых молекул. Перечисленные функции белков стресса называются шаперонными. При различных видах стресса происходит индукция синтеза таких белков: при перегреве организма (40-44°С), при вирусных заболеваниях, отравлениях солями тяжелых металлов, этанолом и др.
В организме южных народов установлено повышенное содержание белков стресса, по сравнению с северной расой.
Молекула белка теплового шока состоит из двух компактных глобул, соединенных свободной цепью:
 Разные белки
теплового шока имеют общий план построения. Все они содержат контактные домены.
Разные белки
теплового шока имеют общий план построения. Все они содержат контактные домены.
Разные белки с различными функциями могут содержать одинаковые домены. Например, различные кальций-связывающие белки имеют одинаковый для всех них домен, отвечающий за связывание Ca +2 .
Роль доменной структуры заключается в том, что она предоставляет белку большие возможности для выполнения своей функции благодаря перемещениям одного домена по отношению к другому. Участки соединения двух доменов – самое слабое в структурном отношении место в молекуле таких белков. Именно здесь чаще всего происходит гидролиз связей, и белок разрушается.
1. КОВАЛЕНТНЫЕ СВЯЗИ - обычные прочные химические связи.
а) пептидная связь
б) дисульфидная связь
2. НЕКОВАЛЕНТНЫЕ (СЛАБЫЕ) ТИПЫ СВЯЗЕЙ - физико-химические взаимодействия родственных структур. В десятки раз слабее обычной химической связи. Очень чувствительны к физико-химическим условиям среды. Они неспецифичны, то есть соединяются друг с другом не строго определенные химические группировки, а самые разнообразные химические группы, но отвечающие определенным требованиям.
а) Водородная связь
б) Ионная связь
в) Гидрофобное взаимодействие
ПЕПТИДНАЯ СВЯЗЬ.
Формируется за счет COOH-группы одной аминокислоты и NH 2 -группы соседней аминокислоты. В названии пептида окончания названий всех аминокислот, кроме последней, находящейся на «С»-конце молекулы меняются на «ил»
Тетрапептид: валил-аспарагил-лизил-серин
 |
ПЕПТИДНАЯ СВЯЗЬ формируется ТОЛЬКО ЗА СЧЕТ АЛЬФА-АМИНОГРУППЫ И СОСЕДНЕЙ COOH-ГРУППЫ ОБЩЕГО ДЛЯ ВСЕХ АМИНОКИСЛОТ ФРАГМЕНТА МОЛЕКУЛЫ!!! Если карбоксильные и аминогруппы входят в состав радикала, то они никогда(!) не участвуют в формировании пептидной связи в молекуле белка.
Любой белок - это длинная неразветвленная полипептидная цепь, содержащая десятки, сотни, а иногда более тысячи аминокислотных остатков. Но какой бы длины ни была полипептидная цепь, всегда в основе ее - стержень молекулы, абсолютно одинаковый у всех белков. Каждая полипептидная цепь имеет N-конец, на котором находится свободная концевая аминогруппа и С-конец, образованный концевой свободной карбоксильной группой. На этом стержне сидят как боковые веточки радикалы аминокислот. Числом, соотношением и чередованием этих радикалов один белок отличается от другого. Сама пептидная связь является частично двойной в силу лактим-лактамной таутомерии. Поэтому вокруг нее невозможно вращение, а сама она по прочности в полтора раза превосходит обычную ковалентную связь. На рисунке видно, что из каждых трех ковалентных связей в стержне молекулы пептида или белка две являются простыми и допускают вращение, поэтому стержень (вся полипептидная цепь) может изгибаться в пространстве.
Хотя пептидная связь довольно прочная, ее сравнительно легко можно разрушить химическим путем – кипячением белка в крепком растворе кислоты или щелочи в течении 1-3 суток.
К ковалентным связям в молекуле белка помимо пептидной, относится также ДИСУЛЬФИДНАЯ СВЯЗЬ.
Цистеин - аминокислота, которая в радикале имеет SH-группу, за счет которой и образуются дисульфидные связи.
 |
Дисульфидная связь - это ковалентная связь. Однако биологически она гораздо менее устойчива, чем пептидная связь. Это объясняется тем, что в организме интенсивно протекают окислительно-восстановительные процессы. Дисульфидная связь может возникать между разными участками одной и той же полипептидной цепи, тогда она удерживает эту цепь в изогнутом состоянии. Если дисульфидная связь возникает между двумя полипептидами, то она объединяет их в одну молекулу.