Применение
Хотя уран-238 не может быть использован как первичный делящийся материал, из-за высокой энергии нейтронов, необходимых для его деления, он занимает важное место в ядерной отрасли.
Имея высокую плотность и атомный вес, U-238 пригоден для изготовления из него оболочек заряда рефлектора в устройствах синтеза и деления. Тот факт, что он делится быстрыми нейтронами, увеличивает энерговыход заряда: косвенно, размножением отраженных нейтронов; непосредственно при делении ядер оболочки быстрыми нейтронами (при синтезе). Примерно 40% нейтронов, образованных при делении и все нейтроны синтеза обладают достаточными для деления U-238 энергиями.
U-238 имеет интенсивность спонтанного деления в 35 раз более высокую, чем U-235, 5.51 делений/с*кг. Это делает невозможным применение его в качестве оболочки заряда рефлектора в пушечных бомбах, ибо подходящая его масса (200-300 кг) создаст слишком высокий нейтронный фон.
Чистый U-238 имеет удельную радиоактивность 0.333 микрокюри/г.
Важная область применения этого изотопа урана - производство плутония-239. Плутоний образуется в ходе нескольких реакций, начинающихся после захвата атомом U-238 нейтрона. Любое реакторное топливо, содержащее природный или частично обогащенный по 235-му изотопу уран, после окончания топливного цикла содержит в себе определенную долю плутония.
Цепочка распада урана-238
Изотоп уран-238, его в природном уране больше, чем 99 %. Этот изотоп является и самым устойчивым, тепловыми нейтронами его ядро расщепить нельзя. Для того, чтобы разделить 238U, нейтрону нужна дополнительная кинетическая энергия 1.4 МэВ. Ядерный реактор из чистого урана-238 ни при каких условиях работать не будет.
Атом урана-238, в ядре которого протоны и нейтроны едва удерживаются вместе силами сцепления. Время от времени из него вырывается компактная группа из четырех частиц: двух протонов и двух нейтронов (б-частица). Уран-238 превращается, таким образом, в торий-234, в ядре которого содержатся 90 протонов и 144 нейтрона. Но торий-234 также нестабилен. Его превращение происходит, однако, не так, как в предыдущем случае: один из его нейтронов превращается в протон, и торий-234 превращается в протактиний-234, в ядре которого содержатся 91 протон и 143 нейтрона. Эта метаморфоза, произошедшая в ядре, сказывается и на движущихся по своим орбитам электронах: один из них становится неспаренным и вылетает из атома. Протактиний очень нестабилен, и ему требуется совсем немного времени на превращение. Далее следуют иные превращения, сопровождаемые излучениями, и вся эта цепочка, в конце концов, оканчивается стабильным нуклидом свинца (смотреть рисунок № 7, приложение Б).
Важнейшим обстоятельством для ядерной энергетики оказывается то, что наиболее распространённый изотоп урана238U тоже является потенциальным источником ядерного горючего. И Сциллард, и Ферми были правы, предполагая, что поглощение нейтронов ураном приведёт к образованию новых элементов. Действительно, при столкновении с тепловым нейтроном уран-238 не делится, вместо этого ядро поглощает нейтрон. В среднем за 23.5 минуты один из нейтронов в ядре превращается в протон (с вылетом электрона, реакция в - распада), и ядроурана-239 становится ядром нептуния-239 (239Np). Через 2.4 суток происходит второй в - распад и образуется плутоний-239 (239Pu).
В результате последовательного поглощения нейтронов в ядерном реакторе могут быть наработаны элементы ещё более тяжёлые, чем плутоний.
В природных минералах и урановой руде обнаруживались только микроколичества 239Pu, 244Pu и 237Np, так что в естественной среде трансурановые элементы (более тяжёлые, чем уран), практически не встречаются.
Изотопы урана, существующие в природе, не совсем стабильны по отношению к б-распаду и спонтанному делению, однако распадаются очень медленно: период полураспада урана-238 равен 4.5 миллиардам лет, а урана-235 - 710 миллионам лет. Из-за малой частоты ядерных реакций такие долгоживущие изотопы не являются опасными источниками радиации. Слиток природного урана можно держать в руках без вреда для здоровья. Его удельная активность равна 0.67 мКи/кг (Ки - кюри, внесистемная единица активности, равная 3.7*1010распадов за секунду).
Деление ядра - это расщепление тяжелого атома на два фрагмента примерно равной массы, сопровождаемое выделением большого количества энергии.
Открытие ядерного деления начало новую эру - «атомный век». Потенциал возможного его использования и соотношение риска к пользе от его применения не только породили множество социологических, политических, экономических и научных достижений, но также и серьезные проблемы. Даже с чисто научной точки зрения процесс ядерного деления создал большое число головоломок и осложнений, и полное теоретическое его объяснение является делом будущего.
Делиться - выгодно
Энергии связи (на нуклон) у разных ядер различаются. Более тяжелые обладают меньшей энергией связи, чем расположенные в середине периодической таблицы.
Это означает, что тяжелым ядрам, у которых атомное число больше 100, выгодно делиться на два меньших фрагмента, тем самым высвобождая энергию, которая превращается в кинетическую энергию осколков. Этот процесс называется расщеплением
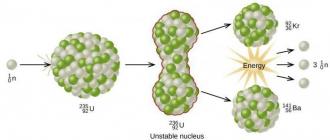
В соответствии с кривой стабильности, которая показывает зависимость числа протонов от числа нейтронов для стабильных нуклидов, более тяжелые ядра предпочитают большее число нейтронов (по сравнению с количеством протонов), чем более легкие. Это говорит о том, что наряду с процессом расщепления будут испускаться некоторые «запасные» нейтроны. Кроме того, они будут также принимать на себя часть выделяющейся энергии. Изучение деления ядра атома урана показало, что при этом выделяется 3-4 нейтрона: 238 U → 145 La + 90 Br + 3n.
Атомное число (и атомная масса) осколка не равна половине атомной массы родителя. Разница между массами атомов, образовавшихся в результате расщепления, обычно составляет около 50. Правда, причина этого еще не совсем понятна.
Энергии связи 238 U, 145 La и 90 Br равны 1803, 1198 и 763 МэВ соответственно. Это означает, что в результате данной реакции высвобождается энергия деления ядра урана, равная 1198 + 763-1803 = 158 МэВ.
Самопроизвольное деление
Процессы спонтанного расщепления известны в природе, но они очень редки. Среднее время жизни указанного процесса составляет около 10 17 лет, а, например, среднее время жизни альфа-распада того же радионуклида составляет около 10 11 лет.
Причина этого заключается в том, что для того, чтобы разделиться на две части, ядро должно сначала подвергнуться деформации (растянуться) в эллипсоидальную форму, а затем, перед окончательным расщеплением на два фрагмента, образовать «горлышко» посредине.

Потенциальный барьер
В деформированном состоянии на ядро действуют две силы. Одна из них - возросшая поверхностная энергия (поверхностное натяжение капли жидкости объясняет ее сферическую форму), а другая - кулоновское отталкивание между осколками деления. Вместе они производят потенциальный барьер.
Как и в случае альфа-распада, чтобы произошло спонтанное деление ядра атома урана, фрагменты должны преодолеть этот барьер с помощью квантового туннелирования. Величина барьера составляет около 6 МэВ, как и в случае с альфа-распадом, но вероятность туннелирования α-частицы значительно больше, чем гораздо более тяжелого продукта расщепления атома.

Вынужденное расщепление
Гораздо более вероятным является индуцированное деление ядра урана. В этом случае материнское ядро облучается нейтронами. Если родитель его поглощает, то они связываются, высвобождая энергию связи в виде колебательной энергии, которая может превысить 6 МэВ, необходимых для преодоления потенциального барьера.
Там, где энергии дополнительного нейтрона недостаточно для преодоления потенциального барьера, падающий нейтрон должен обладать минимальной кинетической энергией для того, чтобы иметь возможность индуцировать расщепление атома. В случае 238 U энергии связи дополнительных нейтронов не хватает около 1 МэВ. Это означает, что деление ядра урана индуцируется только нейтроном с кинетической энергией больше 1 МэВ. С другой стороны, изотоп 235 U имеет один непарный нейтрон. Когда ядро поглощает дополнительный, он образует с ним пару, и в результате этого спаривания появляется дополнительная энергия связи. Этого достаточно для освобождения количества энергии, необходимого для того, чтобы ядро преодолело потенциальный барьер и деление изотопа происходило при столкновении с любым нейтроном.

Бета-распад
Несмотря на то что при реакции деления испускаются три или четыре нейтрона, осколки по-прежнему содержат больше нейтронов, чем их стабильные изобары. Это означает, что фрагменты расщепления, как правило, неустойчивы по отношению к бета-распаду.
Например, когда происходит деление ядра урана 238 U, стабильным изобаром с А = 145 является неодим 145 Nd, что означает, что фрагмент лантан 145 La распадается в три этапа, каждый раз излучая электрон и антинейтрино, пока не будет образован стабильный нуклид. Стабильным изобаром с A = 90 является цирконий 90 Zr, поэтому осколок расщепления бром 90 Br распадается в пять этапов цепи β-распада.
Эти цепи β-распада выделяют дополнительную энергию, которая почти вся уносится электронами и антинейтрино.

Ядерные реакции: деление ядер урана
Прямое излучение нейтрона из нуклида со слишком большим их количеством для обеспечения стабильности ядра маловероятно. Здесь дело заключается в том, что нет кулоновского отталкивания, и поэтому поверхностная энергия имеет тенденцию к удержанию нейтрона в связи с родителем. Тем не менее это иногда происходит. Например, фрагмент деления 90 Br в первой стадии бета-распада производит криптон-90, который может быть находиться в возбужденном состоянии с достаточной энергией, чтобы преодолеть поверхностную энергию. В этом случае излучение нейтронов может происходить непосредственно с образованием криптона-89. по-прежнему неустойчив по отношению к β-распаду, пока не перейдет в стабильный иттрий-89, так что криптон-89 распадается в три этапа.

Деление ядер урана: цепная реакция
Нейтроны, испускаемые в реакции расщепления, могут быть поглощены другим ядром-родителем, которое затем само подвергается индуцированному делению. В случае урана-238 три нейтрона, которые возникают, выходят с энергией менее 1 МэВ (энергия, выделяющаяся при делении ядра урана - 158 МэВ - в основном переходит в кинетическую энергию осколков расщепления), поэтому они не могут вызвать дальнейшее деление этого нуклида. Тем не менее при значительной концентрации редкого изотопа 235 U эти свободные нейтроны могут быть захвачены ядрами 235 U, что действительно может вызвать расщепление, так как в этом случае отсутствует энергетический порог, ниже которого деление не индуцируется.
Таков принцип цепной реакции.

Типы ядерных реакций
Пусть k - число нейтронов, произведенное в образце делящегося материала на стадии n этой цепи, поделенное на число нейтронов, образованных на стадии n - 1. Это число будет зависеть от того, сколько нейтронов, полученных на стадии n - 1, поглощаются ядром, которое может подвергнуться вынужденному делению.
Если k < 1, то цепная реакция просто выдохнется и процесс остановится очень быстро. Именно это и происходит в природной в которой концентрация 235 U настолько мала, что вероятность поглощения одного из нейтронов этим изотопом крайне ничтожна.
Если k > 1, то цепная реакция будет расти до тех пор, пока весь делящийся материал не будет использован Это достигается путем обогащения природной руды до получения достаточно большой концентрации урана-235. Для сферического образца величина k увеличивается с ростом вероятности поглощения нейтронов, которая зависит от радиуса сферы. Поэтому масса U должна превышать некоторую чтобы деление ядер урана (цепная реакция) могло происходить.
Если k = 1, то имеет место управляемая реакция. Это используется в Процесс контролируется распределением среди урана стержней из кадмия или бора, которые поглощают большую часть нейтронов (эти элементы обладают способностью захватывать нейтроны). Деление ядра урана контролируется автоматически путем перемещения стержней таким образом, чтобы величина k оставалась равной единице.
Содержание статьи
УРАН, U (uranium), металлический химический элемент семейства актиноидов, которые включают Ac, Th, Pa, U и трансурановые элементы (Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr). Уран приобрел известность благодаря использованию его в ядерном оружии и атомной энергетике. Оксиды урана применяются также для окрашивания стекла и керамики.
Нахождение в природе.
Содержание урана в земной коре составляет 0,003%, он встречается в поверхностном слое земли в виде четырех видов отложений. Во-первых, это жилы уранинита, или урановой смолки (диоксид урана UO 2), очень богатые ураном, но редко встречающиеся. Им сопутствуют отложения радия, так как радий является прямым продуктом изотопного распада урана. Такие жилы встречаются в Заире, Канаде (Большое Медвежье озеро), Чехии и Франции. Вторым источником урана являются конгломераты ториевой и урановой руды совместно с рудами других важных минералов. Конгломераты обычно содержат достаточные для извлечения количества золота и серебра, а сопутствующими элементами становятся уран и торий. Большие месторождения этих руд находятся в Канаде, ЮАР, России и Австралии. Третьим источником урана являются осадочные породы и песчаники, богатые минералом карнотитом (уранил-ванадат калия), который содержит, кроме урана, значительное количество ванадия и других элементов. Такие руды встречаются в западных штатах США. Железоурановые сланцы и фосфатные руды составляют четвертый источник отложений. Богатые отложения обнаружены в глинистых сланцах Швеции. Некоторые фосфатные руды Марокко и США содержат значительные количества урана, а фосфатные залежи в Анголе и Центральноафриканской Республике еще более богаты ураном. Большинство лигнитов и некоторые угли обычно содержат примеси урана. Богатые ураном отложения лигнитов обнаружены в Северной и Южной Дакоте (США) и битумных углях Испании и Чехии.
Открытие.
Уран был открыт в 1789 немецким химиком М.Клапротом, который присвоил имя элементу в честь открытия за 8 лет перед этим планеты Уран. (Клапрот был ведущим химиком своего времени; он открыл также другие элементы, в том числе Ce, Ti и Zr.) В действительности вещество, полученное Клапротом, было не элементным ураном, но окисленной формой его, а элементный уран был впервые получен французским химиком Э.Пелиго в 1841. С момента открытия и до 20 в. уран не имел того значения, какое он имеет сейчас, хотя многие его физические свойства, а также атомная масса и плотность были определены. В 1896 А.Беккерель установил, что соли урана обладают излучением, которое засвечивает фотопластинку в темноте. Это открытие активизировало химиков к исследованиям в области радиоактивности и в 1898 французские физики супруги П.Кюри и М.Склодовская-Кюри выделили соли радиоактивных элементов полония и радия, а Э.Резерфорд, Ф.Содди, К.Фаянс и другие ученые разработали теорию радиоактивного распада, что заложило основы современной ядерной химии и атомной энергетики.
Первые применения урана.
Хотя радиоактивность солей урана была известна, его руды в первой трети нынешнего столетия использовались лишь для получения сопутствующего радия, а уран считался нежелательным побочным продуктом. Его использование было сосредоточено в основном в технологии керамики и в металлургии; оксиды урана широко применяли для окраски стекла в цвета от бледножелтого до темнозеленого, что способствовало развитию недорогих стекольных производств. Сегодня изделия этих производств идентифицируют как флуоресцирующие под ультрафиолетовыми лучами. Во время Первой мировой войны и вскоре после нее уран в виде карбида применяли в производстве инструментальных сталей, аналогично Mo и W; 4–8% урана заменяли вольфрам, производство которого в то время было ограничено. Для получения инструментальных сталей в 1914–1926 ежегодно производили по нескольку тонн ферроурана, содержащего до 30% (масс.) U. Однако такое применение урана продолжалось недолго.
Современное применение урана.
Промышленность урана начала складываться в 1939, когда было осуществлено деление изотопа урана 235 U, что привело к технической реализации контролируемых цепных реакций деления урана в декабре 1942. Это было рождение эры атома, когда уран из незначительного элемента превратился в один из наиболее важных элементов в жизни общества. Военное значение урана для производства атомной бомбы и использование в качестве топлива в ядерных реакторах вызвали спрос на уран, который возрос в астрономических размерах. Интересна хронология роста потребности в уране по истории отложений в Большом Медвежьем озере (Канада). В 1930 в этом озере была обнаружена смоляная обманка – смесь оксидов урана, а в 1932 на этом участке была налажена технология очистки радия. Из каждой тонны руды (смоляной обманки) получали 1 г радия и около половины тонны побочного продукта – уранового концентрата. Однако радия было мало и его добыча была прекращена. С 1940 по 1942 разработку возобновили и начали отправку урановой руды в США. В 1949 аналогичная очистка урана с некоторыми усовершенствованиями была применена для производства чистого UO 2 . Это производство росло, и в настоящее время оно является одним из наиболее крупных производств урана.
Свойства.
Уран – один из наиболее тяжелых элементов, встречающихся в природе. Чистый металл очень плотный, пластичный, электроположительный с малой электропроводностью и высокореакционноспособный.
Уран имеет три аллотропные модификации: a -уран (орторомбическая кристаллическая решетка), существует в интервале от комнатной температуры до 668° С; b -уран (сложная кристаллическая решетка тетрагонального типа), устойчивый в интервале 668–774° С; g -уран (объемноцентрированная кубическая кристаллическая решетка), устойчивый от 774° С вплоть до температуры плавления (1132° С). Поскольку все изотопы урана нестабильны, все его соединения проявляют радиоактивность.
Изотопы урана
238 U, 235 U, 234 U встречаются в природе в соотношении 99,3:0,7:0,0058, а 236 U – в следовых количествах. Все другие изотопы урана от 226 U до 242 U получают искусственно. Изотоп 235 U имеет особо важное значение. Под действием медленных (тепловых) нейтронов он делится с освобождением огромной энергии. Полное деление 235 U приводит к выделению «теплового энергетического эквивалента» 2Ч 10 7 кВтЧ ч/кг. Деление 235 U можно использовать не только для получения больших количеств энергии, но также для синтеза других важных актиноидных элементов. Уран природного изотопного состава можно использовать в ядерных реакторах для производства нейтронов, образующихся при делении 235 U, в то же время избыточные нейтроны, не востребуемые цепной реакцией, могут захватываться другим природным изотопом, что приводит к получению плутония:
При бомбардировке 238 U быстрыми нейтронами протекают следующие реакции:
Согласно этой схеме, наиболее распространенный изотоп 238 U может превращаться в плутоний-239, который, подобно 235 U, также способен делиться под действием медленных нейтронов.
В настоящее время получено большое число искусственных изотопов урана. Среди них 233 U особенно примечателен тем, что он также делится при взаимодействии с медленными нейтронами.
Некоторые другие искусственные изотопы урана часто применяются в качестве радиоактивных меток (индикаторов) в химических и физических исследованиях; это прежде всего b -излучатель 237 U и a -излучатель 232 U.
Соединения.
Уран – высокореакционноспособный металл – имеет степени окисления от +3 до +6, близок бериллию в ряду активности, взаимодействует со всеми неметаллами и образует интерметаллические соединения с Al, Be, Bi, Co, Cu, Fe, Hg, Mg, Ni, Pb, Sn и Zn. Тонкораздробленный уран особенно реакционноспособен и при температурах выше 500° С часто вступает в реакции, характерные для гидрида урана. Кусковой уран или стружка ярко сгорает при 700–1000° С, а пары урана горят уже при 150–250° С, с HF уран реагирует при 200–400° С, образуя UF 4 и H 2 . Уран медленно растворяется в концентрированной HF или H 2 SO 4 и 85%-ной H 3 PO 4 даже при 90° С, но легко реагирует с конц. HCl и менее активно с HBr или HI. Наиболее активно и быстро протекают реакции урана с разбавленной и концентрированной HNO 3 с образованием нитрата уранила (см. ниже ). В присутствии HCl уран быстро растворяется в органических кислотах, образуя органические соли U 4+ . В зависимости от степени окисления уран образует несколько типов солей (наиболее важные среди них с U 4+ , одна из них UCl 4 – легко окисляемая соль зеленого цвета); соли уранила (радикала UO 2 2+) типа UO 2 (NO 3) 2 имеют желтую окраску и флуоресцируют зеленым цветом. Соли уранила образуются при растворении амфотерного оксида UO 3 (желтая окраска) в кислой среде. В щелочной среде UO 3 образует уранаты типа Na 2 UO 4 или Na 2 U 2 O 7 . Последнее соединение («желтый уранил») применяют для изготовления фарфоровых глазурей и в производстве флуоресцентных стекол.
Галогениды урана широко изучались в 1940–1950, так как на их основе были разработаны методы разделения изотопов урана для атомной бомбы или ядерного реактора. Трифторид урана UF 3 был получен восстановлением UF 4 водородом, а тетрафторид урана UF 4 получают разными способами по реакциям HF с оксидами типа UO 3 или U 3 O 8 или электролитическим восстановлением соединений уранила. Гексафторид урана UF 6 получают фторированием U или UF 4 элементным фтором либо действием кислорода на UF 4 . Гексафторид образует прозрачные кристаллы с высоким коэффициентом преломления при 64° С (1137 мм рт. ст.); соединение летуче (в условиях нормального давления возгоняется при 56,54° С). Оксогалогениды урана, например, оксофториды, имеют состав UO 2 F 2 (фторид уранила), UOF 2 (оксид-дифторид урана).
Уран
Уран, элемент с порядковым
номером 92, самый тяжелый из встречающихся в природе. Использовался он еще
в начале нашей эры, осколки керамики с желтой глазурью (содержащие более
1% оксида урана) находились среди развалин Помпеи и Геркуланума.
Уран был открыт в 1789 году в урановой смолке
немецким химиком Мартоном Генрихом Клапротом, назвавшего его в честь
планеты уран, открытой в 1781. Впервые получил металлический уран
французский химик Юджин Пелиго в 1841, восстановив безводный тетрахлорид
урана калием. В 1896 году Антуан-Анри Беккерель открывает явление
радиоактивности урана случайным засвечиванием фотопластинок ионизирующим
излучением от оказавшегося поблизости кусочка соли урана.
Химические и физические свойства
Уран
очень тяжелый, серебристо-белый глянцеватый металл. В чистом виде он
немного мягче стали, ковкий, гибкий, обладает небольшими парамагнитными
свойствами. Уран имеет три аллотропные формы: альфа (призматическая,
стабильна до 667.7 °C), бета (четырехугольная, стабильна от 667.7 до 774.8
°C), гамма (с объемно центрированной кубической структурой, существующей
от 774.8 °C до точки плавления), в которых уран наиболее податлив и удобен
для обработки. Альфа-фаза - очень примечательный тип призматической
структуры, состоящей из волнистых слоев атомов в чрезвычайно асимметричной
призматической решетке. Такая анизотропная структура затрудняет сплав
урана с другими металлами. Только молибден и ниобий могут создавать с
ураном твердофазные сплавы. Правда, металлический уран может вступать во
взаимодействие со многими сплавами, образуя интерметаллические
соеденинения.
Основные физические
свойства урана:
температура плавления 1132.2 °C (+/- 0.8);
температура кипения 3818 °C;
плотность 18.95 (в альфа-фазе);
удельная теплоемкость 6.65 кал/моль/°C (25 C);
прочность на разрыв
450 МПа.
Химически уран очень
активный металл. Быстро окисляясь на воздухе, он покрывается радужной
пленкой оксида. Мелкий порошок урана самовоспламеняется на воздухе, он
зажигается при температуре 150-175 °C, образуя U 3 O 8 .
При 1000 °C уран соединяется с азотом, образуя желтый нитрид урана. Вода
способна разъедать металл, медленно при низкой температуре, и быстро при
высокой. Уран растворяется в соляной, азотной и других кислотах, образуя
четырехвалентные соли, зато не взаимодействует с щелочами. Уран вытесняет
водород из неорганических кислот и солевых растворов таких металлов как
ртуть, серебро, медь, олово, платина и золото. При сильном встряхивании
металлические частицы урана начинают светиться.
Уран имеет четыре степени окисления - III-VI.
Шестивалентные соединения включают в себя триокись уранила UO 3
и уранилхлорид урана UO 2 Cl 2 . Тетрахлорид урана
UCl 4 и диоксид урана UO 2 - примеры четырехвалентного
урана. Вещества, содержащие четырехвалентный уран обычно нестабильны и
обращаются в шестивалентные при длительном пребывании на воздухе.
Ураниловые соли, такие как уранилхлорид распадаются в присутствии яркого
света или органики.
Изотопы урана
Уран имеет 14 изотопов, при
этом только три из них встречаются в природе. Примерный изотопный состав
природного урана следующий:
Хотя
содержание изотопа U-235 в общем постоянно, могут иметься некоторые
колебания его количества, в следствии обеднения руды из-за реакций
деления, имевших место, когда концентрация U-235 была много выше, чем
сегодня. Самый известный такой природный "реактор", возрастом 1.9
миллиарда лет, обнаружен в 1972 году в шахте Окло в Габоне. Когда этот
реактор действовал, в природном уране содержалось 3% U-235, столько же,
сколько и в современном топливе для атомных электростанций. Теперь ядро
шахты выгорело и обеднено, содержит лишь 0.44% U-235. Естественные
реакторы в Окло и несколько еще, открытых поблизости, являются
единственными в своем роде до сих пор.
Содержание U-234 в руде очень незначительно. В
отличие от U-235 и U-238, из-за своей короткой жизни, все количество этого
изотопа образуется вследствии распада атомов U-238:
U 238
-> (4.51 миллиарда лет, альфа-распад) -> Th 234
Th 234 -> (24.1 дней, бета-распад) -> Pa 234
Pa 234 -> (6.75 часов, бета-распад) -> U 234
Обычно U-234 существует в равновесии с U-238,
распадаясь и образуясь с одинаковой скоростью. Однако распадающиеся атомы
U-238 существуют некоторое время в виде тория и протактиния, поэтому могут
химически или физически отделиться от руды (выщелачиваться подземными
водами). Поскольку U-234 обладает относительно коротким временем
полураспада, весь этот изотоп, находящийся в руде, образовался в последние
несколько миллионов лет. Примерно половину радиоактивности природного
урана составляет вклад U-234.
U-236 обладает
периодом полураспада 23.9 миллиона лет и не встречается в природе в
значительных количествах. Он накапливается, если уран облучается
нейтронами в реакторах, и потому используется как "сигнализатор"
отработанного уранового ядерного топлива.
Удельная радиоактивность природного урана 0.67 микрокюри/г (разделяется практически пополам между U-234 и U-238, U-235 вносит маленький вклад). Природный уран достаточно радиоактивен для засвечивания фотопластинки за время около часа.
U-235.
В природном уране только один, относительно
редкий, изотоп подходит для изготовления ядра атомной бомбы или
поддержания реакции в энергетическом реакторе. Степень обогащения по U-235
в ядерном топливе для АЭС колеблется в пределах 2-4.5%, для оружейного
использования - минимум 80%, а более предпочтительно 90%. В США уран-235
оружейного качества обогащен до 93.5%, промышленность способна выдавать
97.65% - уран такого качества используется в реакторах для военно-морского
флота.
В 1998 году изотопное отделение
Ок-Риджской Национальной лаборатории (ORNL) поставляло 93% U-235 по цене
53$/г.
Будучи еще более легким, U-234
пропорционально обогащается даже еще в большей степени, чем U-235 во всех
процессах разделения, основанных на разнице в массах. Высокообогащенный
U-235 обычно содержит 1.5-2.0% U-234.
Интенсивность спонтанного деления U-235 0.16
делений/с*кг. Чистая 60-килограмовая масса U-235 производит всего 9.6
делений/с, делая достаточно простой для изготовления пушечную схему. U-238
создает в 35 раз больше нейтронов на килограмм, так что даже маленький
процент этого изотопа поднимает этот показатель в несколько раз. U-234
создает в 22 раза больше нейтронов и имеет похожее с U-238 нежелательное
действие.
Удельная активность U-235 всего 2.1
микрокюри/г; загрязнение его 0.8% U-234 поднимают ее до 51 микрокюри/г.
U-238.
Хотя уран-238 не может быть использован как
первичный делящийся материал, из-за высокой энергии нейтронов, необходимых
для его деления, он занимает важное место в ядерной отрасли.
Имея высокую плотность и атомный вес, U-238
пригоден для изготовления из него оболочек заряда/рефлектора в устройствах
синтеза и деления. Тот факт, что он делится быстрыми нейтронами,
увеличивает энерговыход заряда: косвенно, размножением отраженных
нейтронов; непосредственно при делении ядер оболочки быстрыми нейтронами
(при синтезе). Примерно 40% нейтронов, образованных при делении и все
нейтроны синтеза обладают достаточными для деления U-238 энергиями.
U-238 имеет интенсивность спонтанного деления
в 35 раз более высокую, чем U-235, 5.51 делений/с*кг. Это делает
невозможным применение его в качестве оболочки заряда/рефлектора в
пушечных бомбах, ибо подходящая его масса (200-300 кг) создаст слишком
высокий нейтронный фон.
Чистый U-238 имеет
удельную радиоактивность 0.333 микрокюри/г.
Важная область применения этого изотопа урана
- производство плутония-239. Плутоний образуется в ходе нескольких
реакций, начинающихся после захвата атомом U-238 нейтрона. Любое
реакторное топливо, содержащее природный или частично обогащенный по
235-му изотопу уран, после окончания топливного цикла содержит в себе
определенную долю плутония.
U-233 и U-232.
Этот изотоп урана с периодом полураспада 162
000 лет не встречается в природе. Его можно получить из тория-232,
облучением нейтронами, наподобии производства плутония:
Th 232 + n -> Th 233
Th 233 ->
(22.2 м, бета-распад) -> Pa 233
Pa 233 ->
(27.0 дней, бета-распад) -> U 233
Наряду с этой, может
протекать двухстадийная побочная реакция, венчающаяся образованием U-232:
Th 232 + n -> T 231 + 2n
Th 231
-> (25.5 ч, бета-распад) -> Pa 231
Pa 231 +
n -> Pa 232
Pa 232 -> (1.31 дней,
бета-распад) -> U 232
Наработка урана-232 в ходе этой
реакции зависит от присутствия в значительных количествах быстрых
(нетепловых) нейтронов, ибо сечение первой реакции этого цикла слишком
мало для тепловых скоростей. Если в исходном веществе находится Th-230, то
образование U-232 дополняется реакцией:
Th 230 + n ->
Th 231
и далее как указано выше.
Наличие U-232 очень важно из-за
последовательности распада:
U 232 -> (76 лет,
альфа-распад) -> Th 228
Th 228 -> (1.913
лет, альфа-распад) -> Ra 224
Ra 224 -> (3.64
дней, альфа- и гамма-распад) -> Rn 220
Rn 220
-> (55.6 с, альфа-распад) -> Po 216
Po 216
-> (0.155 с, альфа-распад) -> Pb 212
P -212
-> (10.64 ч, бета- и гамма-распад) -> Bi 212
Bi 212 -> (60.6 мин, бета- и гамма-распад) ->
Po 212
альфа-
и гамма-распад) -> Tl 208
Po 212 ->
(3x10 -7 с, альфа-распад) -> Pb 208 (стабилен)
Tl 208 -> (3.06 мин, бета- и гамма-распад) ->
Pb 208
Большое количество энергичных гамма-лучей выделяется
с началом быстрой последовательности распада Ra-224. Около 85% всей общей
энергии образуется при распаде последнего члена последовательности -
тантала-208 - энергия гамма-лучей до 2.6 МэВ.
Накопление U-232 неизбежно при производстве
U-233. Это аналогично накоплению помимо Pu-239 других изотопов плутония,
только в гораздо меньшей степени. Первая реакция цикла требует нейтронов с
энергией не менее 6 МэВ. Такими энергиями обладает очень небольшое
количество нейтронов деления и если зона воспроизводства тория находится в
такой части реактора, где она облучается умеренно быстрыми нейтронами (~
500 кэВ) эта реакция может быть практически исключена. Вторая реакция (с
Th-230) превосходно идет и с тепловыми нейтронами. Отсюда снижение
образования U-232 требует загрузки тория с минимальной концентрацией
Th-230.
Вышеописанные меры предосторожности
ведут к содержанию в оружейном U-233 U-232 в количестве 5 частей на
миллион (0.0005%).
В коммерческом ядерном
топливном цикле сосредоточение U-232 не представляет собой большого
недостатка, даже желательно, поскольку это снижает возможность
распространения урана для оружейных целей. Для экономии топлива, после его
переработки и повторного использования уровень U-232 достигает 0.1-0.2%. В
специально спроектированных системах этот изотоп накапливается в
концентрациях 0.5-1%.
В течении первых пары
лет после производства U-233, содержащего U-232, Th-228 сохраняется на
постоянном уровне, находясь в равновесии с собственным распадом. В этом
периоде фоновое значение гамма-излучения устанавливается и
стабилизируется. Таким образом, первые несколько лет произведенная масса
U-233 может испускать значительное гамма-излучение. Десятикилограммовая
сфера U-233 оружейной чистоты (5 миллионных долей U-232) создает фон 11
миллибэр/час на расстоянии 1 м спустя 1 месяц после производства, 110
миллибэр/ч через год, 200 миллибэр/ч через 2 года. Обычная камера с
перчатками, используемая для сборки ядер бомб, быстро создает трудности с
безопасностью для сотрудников. Ежегодная предельная доза в 5 бэр
превышается уже через 25 часов работы с таким материалом. Даже свежий
U-233 (1 месяц со дня изготовления) ограничивает время сборки десятью
часами в неделю.
В полностью собранном оружии
уровень радиации может снижаться поглощением корпусом заряда. В
современных облегченных устройствах снижение не превышает 10 раз, создавая
проблемы с безопасностью. В более тяжеловесных зарядах поглощение много
более сильное - в 100 - 1000 раз. Рефлектор из бериллия увеличивает
уровень нейтронного фона:
Be 9 + гамма-квант ->
Be 8 + нейтрон
Гамма-лучи U-232 образуют характерную
сигнатуру, их можно обнаружить и отследить передвижения и наличие атомного
заряда.
Производимый по ториевому циклу
специально денатурировонный U-233 (0.5 - 1.0% U-232), создает еще большую
опасность. Такая же 10-килограмовая сфера, как описанная выше, только
изготовленная из такого материала, на расстоянии 1 м через 1 месяц создает
фон 11 бэр/час, 110 бэр/ч через год и 200 бэр/ч через 2 года. Обработка и
изготовление такого урана идет только в специальных боксах, с применением
механических манипуляторов (они используются при создании тепловыделяющих
сборок для атомных станций). Если попытаться произвести атомную бомбу из
этого вещества, даже при сокращении излучения в 1000 раз, непосредственный
контакт с таким изделием ограничивается 25 часами в год. Таким образом,
наличие заметной доли U-232 в делящемся веществе делает его крайне
неудобным для военного применения.
Короткий
период полураспада у U-232 делает его очень активным источником
альфа-частиц. U-233 с 1% U-232 имеет в три раза более сильную
альфа-радиоактивность, чем оружейный плутоний и, соответственно, большую
радиотоксичность. Эта альфа-активность вызывает рождение нейтронов в
легких элементах заряда, представляя даже более серьезную проблему, чем
реакция бериллия с гамма-квантами. Для минимизации этой проблемы
присутствие таких элементов как бериллий, бор, фтор, литий должно быть как
можно меньшим. Наличие нейтронного фона совершенно не влияет на
имплозионные системы, так как он все равно меньше, чем у плутония. Для
пушечных проектов требуемый уровень чистоты по легким материалам - одна
часть к миллиону. Хотя такая очистка урана нетривиальная задача, она не
выходит за рамки стандартных химических методов очистки. Это демонстрируют
хотя бы возможности электронной промышленности по изготовлению кремния
даже более высокой чистоты.
U-233 имеет
интенсивность спонтанного деления 0.47 делений/с*кг. U-233 имеет
интенсивность спонтанного деления 720 делений/с*кг. Удельная
радиоактивность U-233 9.636 милликюри/г, давая альфа-активность (и
радиотоксичность) примерно 15% от плутония. Всего 1% U-232 увеличивает
радиоактивность до 212 милликюри/г.
Несмотря
на недостаток в виде сильной гамма- и нейтронной радиоактивности, U-233 -
прекрасный делящийся материал для ядра атомной бомбы. Он обладает меньшей
критической массой, чем U-235 и его ядерные характеристики сходны с
плутонием. США производили испытания зарядов на основе U-233 в операции
Teapot в 1957 году. Индия придает большое значение U-233 как части
исследования и производства оружия и официально включила производство
изотопа в свою ядерную программу.
Обедненный уран.
После извлечения U-235 из природного урана,
оставшийся материал носит название "обедненный уран", т.к. он обеднен
235-ым изотопом. В США хранится около 560 000 тонн обедненного
гексафторида урана (UF 6) на трех газодиффузионных
обогатительных производствах минэнергетики США: в г. Падьюка (Paducah),
штат Кентукки; в г. Портсмут (Portsmouth), Огайо; и в Ок-Ридже (Oak
Ridge), Теннесси.
Обедненный уран в два раза
менее радиоактивен, чем природный уран, в основном за счет удаления из
него U-234. Из-за того, что основное использование урана - производство
энергии, обедненный уран бесполезный продукт с низкой экономическое
ценностью. Нахождение путей использования обедненного урана представляет
собой большую проблему для обогатительных предприятий.
В основном его использование связано с большой
плотностью урана и относительно низкой его стоимостью. Две важнейшие сферы
использования обедненного урана: использование его для радиационной защиты
(как это не странно) и как балластная масса в аэрокосмических применениях,
таких как рулевые поверхности летательных аппаратов. В каждом самолете
Боинг-747 содержится 1500 кг обедненного урана для этих целей. Обедненный
уран в значительной степени применяется при бурении нефтяных скважин в
виде ударных штанг (при канатном бурении), его вес погружает инструмент в
скважины, наполненые буровым раствором. Еще этот материал применяется в
высокоскоростных роторах гироскопов, больших маховиках, как балласт в
космических спускаемых аппаратах и гоночных яхтах.
Но самое известное применение урана - в
качестве сердечников для американских бронебойных снарядов. При
определенном сплаве с другими металлами и термической обработке
(сплавление с 2% Mo или 0.75% Ti, быстрая закалка разогретого до 850 °С
металла в воде или масле, дальнейшее выдерживание при 450 °С 5 часов)
металлический уран становиться тверже и прочнее стали (прочность на разрыв
> 1600 МПа). В сочитании с большой плотностью, это делает закаленный
уран чрезвычайно эффективным для пробивания брони, аналогичным по
эффективности много более дорогому монокристаллическому вольфраму. Процесс
разрушения брони сопровождается измельчением в пыль большинства урана,
проникновением пыли внутрь защищенного объекта и воспламенением ее на
воздухе с другой стороны. Около 300 тонн обедненного урана остались на
поле боя во время Бури в Пустыне (по большей части это остатки снарядов
30-мм пушки GAU-8 штурмовых самолетов A-10, каждый снаряд содержит 272 г
уранового сплава).
Обедненный уран
используется в современной танковой броне, например, танка M-1 "Абрамс".
Захват нейтронов U-235 и U-238
Обогащение урана
Во время Манхэттенского
проекта природный уран получил название "tuballoy" (сокращенно "Tu") из-за
подразделения проекта "Tube Alloy Division", это название все еще иногда
встречается в отношении природного или обедненного урана. Кодовое имя
высокообогащенного урана (особенно оружейного обогащения) - "oralloy"
(сокращенно "Oy"). Названия "Q-metal", "depletalloy", и "D-38" относятся
только к обедненному урану.
Практически важное
соединение урана - гексафторид урана UF 6 . Это единственное
стабильное и легколетучее соединение урана, использующееся при разделении
его изотопов - газовой диффузии и центрифугировании. В этом аспекте его
применения важно и то, что фтор имеет всего один изотоп (это не вносит
дополнительной усложняющей разницы в массах) и то, что UF 6 -
стехиометрическое соединение (состоящее в точности из 6 атомов фтора и 1
атома урана). При комнатной температуре оно представляет собой бесцветные
кристаллы, а при нагреве до 56 °С сублимируется (испаряется без перехода в
жидкую фазу). Его температура плавления 64 °C, плотность - 4.87 твердая и
3.86 жидкая фазы. Это фтористое вещество разъедает большинство металлов и
оксидов, кроме алюминия (вследствии наличия тонкой пленки окисла) и никеля
(благодаря образованию пленки фторида никеля). Большая часть оборудования
для работы с гексафторидом урана сделана из алюминия либо покрыта слоем
никеля.
Среди других соединений стоит отметить
и гидрид урана UH 3 . Он изучался в Лос-Аламосе еще в рамках
Манхэттенского проекта как материал для атомной бомбы. По теории,
присутствующие атомы водорода должны замедлять нейтроны до таких
скоростей, при которых сечение поглощения их атомами U-235 было бы гораздо
больше. Хотя это могло бы сделать бомбу менее эффективной, оставалось
надежда на сокращение требуемой массы урана. Уже послевоенные исследования
показали неожиданно низкую плотность гидрида (всего 8) и маленькое
реальное сечение захвата, сделавшие эту схему неработоспособной. Испытания
в 1953 году в операции Upshot-Knothole
имплозионных бомб с ядрами из UH 3 подтвердили это, произведя
очень незначительные "хлопки".
До
второй мировой войны уран считался редким металлом. Сейчас известно, уран
более распространен, чем ртуть или серебро и содержится в промышленных
рудах примерно в таких же концентрациях, как мышьяк или молибден. Его
средняя концентрация в земной коре примерно 2 части к 1 миллиону, занимает
48 место по содержанию в кристаллических породах. В литосфере уран более
распространен, чем такие недорогие вещества как цинк и бор, встречающиеся
в концентрациях 4 г/т. Содержание урана в гранитных породах вполне
достаточное, чтобы радиоактивный газ радон, продукт распада, представлял
серьезную биологическую опасность в местах выхода гранита на поверхность.
Уран обнаружен и в морской воде, в концентрации 150 мкг/м 3 .
Уран входит в достаточной концентрации в 150
различных минералов, и в небольшом количестве - еще в 50. Первоначально
его нашли в магматических гидротермальных жилах и пегматитах, включая
уранинит и смоляную обманку. В этих рудах уран содержится в виде диоксида,
который, в зависимости от степени окисления, имеет средний состав от
UO 2 до UO 2.67 . Еще руды, имеющие экономическое
значение: аутанит, гидраткальциевый уранильный фосфат; тобернит,
гидратмедный уранильный фосфат; коффинит, гидратированный силикат урана;
карнотит, гидраткалиевый уранильный ванадат. Урановые руды имеются по
всему миру. Запасы и коммерческие сделки выражаются в эквивалентных массах
U 3 O 8 . Один килограмм U 3 O 8
стоит в среднем около 40$.
Месторождения
смоляной обманки, самой богатой ураном руды, располагаются главным образом
в Канаде, Конго и США. Большинство из добывающегося в США урана
вырабатывается из получаемого в штатах Юта, Колорадо, Нью-Мексико,
Аризона, Вайоминг карнотита. Минерал, названный коффинит, открытый в 1955
году в Колорадо, очень богатая руда - содержание урана ~61%. Впоследствии
коффинит нашли в Вайоминге и Аризоне. В 1990 году производство уранового
концентрата в США составило 3417 тонн.
Урановые руды содержат обычно
небольшое количество ураносодержащего минерала, так что необходимы
предварительное извлечение и обогащение. Физическое разделение
(гравитация, флотация, электростатика) неприменимо для урана, в дело идут
методы гидрометаллургии - выщелачивание - обычный первый шаг обработки
руды.
В классическом способе кислотного
выщелачивания руда первоначально измельчается и обжигается для
обезвоживания, удаляются углеродсодержащие фракции, сульфатируется,
восстановители, которые могут быть препятствием для выщелачивания
окисляются. Затем смесь обрабатывается серной и азотной кислотами. Уран
переходит в сульфат уранила, радий и другие металлы в урановой смолке
оседают в виде сульфатов. С добавлением едкого натра уран осаждается в
виде диураната натрия
Na 2 U 2 O 7 .6H 2 O.
Классические методы извлечения урана из руды в
настоящее время пополнены такими процедурами как экстракция
растворителями, ионным обменом, выпариванием.
Во время экстракции растворителями урановая
руда удаляется из щелока от выщелачивания подкисленной породы при помощи
смеси растворителей, например р-ра трибутилфосфата в керосине. В
современных промышленных методах в качестве растворителей фигурируют
алкил-фосфорные кислоты (например, ди(2-этилгексил)-фосфорная кислота) и
вторичные и третичные алкиламины.
Как общее
правило, экстракция растворителями предпочитается ионообменным методам при
содержании урана в растворе после кислотного выщелачивания более 1 грамма
на литр. Однако оно неприменимо для восстановления урана из карбонатных
растворов.
Уран, удовлетворяющий условиям
оружейной чистоты, обычно получают из диураната натрия через прохождение
дополнительной очистки, используя трибутилфосфатный очистительный процесс.
Первоначально, Na 2 U 2 O 7 .6H 2 O
растворяют в азотной кислоте для подготовки сырьевого раствора. Из него
избирательно удаляется уран при разбавлении раствора трибутилфосфатом с
керосином или иной подходящей углеводородной смесью. Наконец, уран
переходит из трибутилфосфата в подкисленную воду для выделения
высокоочищенного уранильного нитрата. Нитрат кальцинируется в
UO 3 , который восстанавливается в водородной атмосфере до
UO 2 . UO 2 конвертируется в UF 4 в безводном
фтористом водороде (HF).
Металлический уран
получают восстановлением урановых галлогенидов (обычно тетрафторида урана)
магнием в экзотермической реакции в "бомбе" - герметичном контейнере,
обычно стальном, общая методика известна как "термитный процесс".
Производство металлического урана восстановлением магнием тетрафторида
иногда называют способом Амеса (Ames), в честь университета Айовы, Амеса,
где химик Ф. Х. Спеддинг (F.H. Spedding) и его группа разработали этот
процесс в 1942 году.
Реакции в "бомбе"
протекают при температурах, превышающих 1300 °C. Прочный стальной корпус
необходим, чтобы выдержать высокое давление внутри него. "Бомба"
заряжается гранулами UF 4 и в избытке засыпается тонко
диспергированным магнием и нагревается до 500-700 °C, с этого момента
начинается саморазогревающаяся реакция. Теплоты реакции достаточно для
расплавления начинки "бомбы", состоящей из металлического урана и шлака -
фторида магния MF 2 . Этот самый шлак отделяется и всплывет
вверх. Когда "бомба" охлаждается, получается слиток металлического урана,
который, несмотря на содержание в нем водорода, самый качественный из
коммерчески доступных и хорошо подходит для топлива АЭС.
Металл получается и при восстановлении оксидов
урана кальцием, алюминием или углеродом при высоких температурах; или
электролизом KUF 5 или UF 4 , растворенных в расплаве
CaCl 2 и NaCl. Уран высокой чистоты можно получить термическим
разложением галлогенидов урана на поверхности тонкой нити.
При завершении процесса обогащения урана, обычно в отходах остается 0.25-0.4% U-235, так как извлекать этот изотоп до конца экономически невыгодно (дешевле закупать большее количество сырья). В США остаточное содержание U-235 в сырье после производства возросло с 0.2531% в 1963 до 0.30% в 70-х, по причине снижения стоимости природного урана.
Разделительная способность обогатительного завода измеряется в массе переработанного вещества (МПП) за единицу времени, например МПП-кг/год или МПП-тонн/год. Выход обогащенного продукта с предприятия заданной мощности так же зависит от концентрации нужного изотопа во входной породе, выходных отходах и конечном продукте. Исходное содержание полезного изотопа обычно зафиксировано природным его содержанием. Зато два остальных параметра могут меняться. Если уменьшить степень извлечения изотопа из исходного вещества, можно увеличить скорость его выхода, но платой за это будет увеличение требуемой массы сырья. Это подчиняется отношению:
где P - выход продукта, U - разделительная способность, N P , N F , N W - молярные концентрации изотопа в конечном продукте, сырье и отходах. V(N P), V(N W), V(N F) разделительные потенциальные функции для каждой концентрации. Они определяются как:
![]()
Принимая остаточную концентрацию в 0.25%, завод с производительностью 3100 МПП-кг/год произведет 15 кг 90% U-235 ежегодно из натурального урана. Если взять в качестве сырья трехпроцентный U-235 (топливо для АЭС) и концентрацию 0.7% в отходах производства, тогда достаточно мощности 886 МПП-кг/год для того же выхода.
Методы разделения. Для разделения урана в то или иное время использовались(ются) следующие технологии:
Дополнительного внимания заслуживают следующие, пока промышленно неприменяемые методы:
Подробно эти методы обсуждаются в статье "Методы разделения изотопов" , здесь же приводятся заметки именно относительно урана.
Электромагнитное
разделение.
Это была исторически
первая техника, способная к производству оружейного урана. Она
использовалась в электромагнитном сепараторе Y-12 в Ок-Ридже во время
второй мировой войны. Двух этапов разделения достаточно для обогащения
урана до 80-90%. Два остальных метода, доступных в то время - газовая
диффузия, жидкостная термодиффузия - применялись для начального обогащения
урана и увеличения выхода электромагнитного сепаратора по отношению к
сырью из природного урана. Весь использованный в хиросимской бомбе уран
произведен по этой технологии.
В связи с
высокими накладными расходами Y-12 был закрыт в 1946 году. В более позднее
время только Ирак пытался промышленно использовать этот метод в своей
атомной программе.
Газовая
диффузия.
Первая практически
применяемая в промышленных масштабах технология. Несмотря на требование
наличия для сильного обогащения тысяч ступеней, по затратам это более
выгодный метод, чем электромагнитное разделение. Газодиффузионные
предприятия по обогащению U-235 огромны и имеют большую производственную
мощность.
Главная трудность - создание
надежных газодиффузионных барьеров, способных противостоять коррозийному
действию UF 6 . Есть два основных типа таких барьеров: тонкие
пористые мембраны и барьеры, собранные из отдельных трубочек. Мембраны
представляют собой пленки с образованными травлением порами. Например,
азотная кислота протравливает сплав 40/60 Au/Ag (Ag/Zn); либо
электролитическим травлением алюминиевой фольги можно получить хрупкую
алюминиевую мембрану. Составные барьеры собираются из маленьких дискретных
элементов, упакованных в относительно толстую пористую перегородку.
Технология изготовления диффузионных барьеров
продолжает оставаться засекреченной во всех странах, разработавших ее.
Построенное во время второй мировой войны
производство K-25 в Ок-Ридже состояло из 3024 ступеней обогащения и
продолжало функционировать до конца 1970-х. Разработка подходящего
материала для барьеров оказалась сложным делом, что вызвало некоторую
задержку с вводом в строй предприятия после войны, хотя даже частично
законченный завод внес вклад в накопление U-235 для "Малыша" (Little Boy).
В то время барьеры изготавливались из спеченного никелевого порошка,
попытки создать многообещающие мембраны из электролитически вытравленного
алюминия провалились. K-25 изначально содержал 162 000 м 2
мембранной поверхности. Это предприятие, с расширениями, произвело большую
часть всего урана для армии США в шестидесятых. С усовершенствованием
газодиффузионных барьеров производительность завода возросла в 23 раза.
Диффузионное производство потребляет гораздо
меньше электроэнергии по сравнению с электромагнитным, но ее расход все
равно остается достаточно большим. В 1981 году, после модернизации, оно
имело удельную потребляемую мощность на уровне 2370 кВт-ч/МПП-кг.
Несмотря на то, что уран низкого обогащения -
ценное сырье для производства высокообогащенного урана, газодиффузионные
установки низкого обогащения невозможно легко переделать для производства
урана высокого обогащения. Высокое обогащение требует много меньших по
размеру ступеней, из-за резкого снижения коэффициента обогащения и проблем
с критичностью (накопление критической массы урана) у больших по размеру
блоков.
Огромные размеры обогатительной
системы ведут к длительному времени заполнения ее материалом (обогащаемым
веществом), до начала выхода продукта. Обычно это время установления
равновесия составляет 1-3 месяца.
Технология
газовой диффузии широко использовалась во множестве стран, даже Аргентина
создала действующее обогатительное предприятие для своей тайной оружейной
программы (в настоящее время прекращенной). В 1979 году более 98% всего
урана производилось с использованием этого процесса. К середине 1980-х эта
доля сократилась до 95% с освоением метода центрифугирования.
Жидкостная
термодиффузия.
Жидкостная
термодиффузия оказалась первой технологией, на которой были получены
существенные количества низкообогащенного урана. Она применялась в США во
время Манхэттенского проекта для увеличения КПД сепаратора Y-12. Это самый
простой из всех методов разделения, но предельная степень обогащения по
U-235 всего ~1% (завод S-50 в Ок-Ридже производил 0.85-0.89% урана-235 в
конечном продукте). Кроме того, для термодиффузии нужны огромные
количества тепла.
Газовое
центрифугирование.
Доминирующий способ
разделения изотопов для новых производств, хотя уже существующие мощности
- по большей части газодиффузионные. Каждая центрифуга обеспечивает
гораздо больший коэффициент разделения, чем одна газовая ступень.
Требуется много меньше ступеней, всего около тысячи, правда стоимость
каждой центрифуги гораздо выше.
Газовое
центрифугирование требует ~1/10 часть энергии, требующейся газовой
диффузии (его энергопотребление 100-250 кВт-ч/МПП-кг) и обеспечивает более
легкое наращивание масштаба производства.
Из
развивающихся ядерных стран этой достаточно сложной технологией владеют
Пакистан и Индия.
Аэродинамическая
сепарация.
Аэродинамическое разделение
разработано в ЮАР (процесс UCOR, использующий вихревые трубки с давлением
6 бар) и Германии (используются искривленные сопла, работающие с давлением
0.25-0.5 бар).
Единственная страна,
применявшая этот метод на практике - ЮАР, где было произведено 400 кг
оружейного урана на предприятии в Валиндабе, закрытом в конце
восьмидесятых. Коэффициент разделения ~1.015, энергозатраты ~3300
кВт-ч/МПП-кг.
Испарение с
использованием лазера.
AVLIS (atomic
vapor laser isotope separation). Технология так и не была воплощена в
производстве, разрабатывалась в США в течении 1970-80-х гг. и отмерла
вследствии общего переизбытка разделяющих мощностей и сокращении арсенала.
Химическое разделение.
Химическое разделение урана разрабатывалось в
Японии и Франции, но, как и AVLIS, никогда не использовалось. Французкий
метод Chemex использует противоток в высокой колонне двух несмешиваемых
жидкостей, каждая содержащая растворенный уран. Японский метод Asahi
использует реакцию обмена между водным раствором и мелкоизмельченной
смолой, через которую медленно просачивается раствор. Оба способа
нуждаются в катализаторах для ускорение процесса концентрации. Процесс
Chemex нуждается в электричестве на уровне 600 кВт-ч/МПП-кг.
Ирак разрабатывал эту технологию (в виде
смешанного производства Chemex/Asahi) для обогащения U-235 до 6-8% и
последующем дообогащением в калютроне.
Приблизительные энергетические
эффективности указанных методов по отношению к газовой диффузии:
менее
0.01? AVLIS (если доведена до промышленного употребления)
0.10-0.04
газовое центрифугирование
0.30 химическое разделение
1.00 газовая
диффузия
1.50 аэродинамическая сепарация
высокое электромагнитное
разделение
высокое жидкостная термодиффузия
Перевод Section 6.0 Nuclear Weapons FAQ, Carey Sublette, . Fap suite nero. Керамическая плитка fap luce. . Большие шары стальные. Хорошие шары стальные.
Изучая явление радиоактивности, каждый ученый обращается к такой важнейшей его характеристике как период полураспада. Как известно, гласит, что каждую секунду в мире происходит распад атомов, при этом количественная характеристика этих процессов напрямую связана с количеством имеющихся атомов. Если за определенный период времени произойдет распад половины от всего имеющегося в наличии количества атомов, то распад ½ от оставшихся атомов потребует такого же количества времени. Именно этот временной промежуток и называется периодом полураспада. У разных элементов он различен - от тысячных долей миллисекунды до миллиардов лет, как, например, в случае, когда речь идет про период полураспада урана.
Уран, как самый тяжелый из всех существующих в естественном состоянии элементов на Земле, является вообще самым прекрасным объектом для изучения процесса радиоактивности. Этот элемент был открыт еще в 1789 году немецким ученым М. Клапротом, который дал ему название в честь недавно открытой планеты Уран. То, что уран радиоактивен, было совершенно случайно установлено в конце XIX века французским химиком А. Беккерелем.
Урана рассчитывается по той же формуле, что и аналогичные периоды других радиоактивных элементов:
T_{1/2} = au ln 2 = frac{ln 2}{lambda},
где «au» - среднее время существования атома, «lambda» - основная постоянная распада. Так как ln 2 равен примерно 0,7, то период полураспада лишь на 30% короче в среднем, чем общее время жизни атома.
Несмотря на то, что на сегодняшний день ученым известно 14 изотопов урана, в природе их встречаются только три: уран-234, уран-235 и уран-238. урана различен: так для U-234 он составляет «всего» 270 тысяч лет, а период полураспада урана-238 превышает 4,5 миллиарда. Период полураспада урана-235 находится в «золотой середине» - 710 миллионов лет.
Стоит отметить, что радиоактивность урана в естественных условиях достаточно высока и позволяет, к примеру, засветить фотопластинки в течение всего лишь часа. В то же время стоит отметить, что в из всех изотопов урана только U-235 пригоден для изготовления начинки для Все дело в том, что период полураспада урана-235 в промышленных условиях менее интенсивен, чем его «собратьев», поэтому и выход ненужных нейтронов здесь минимален.
Период полураспада урана-238 значительно превышает 4 миллиарда лет, однако и он сейчас активно используется в атомной промышленности. Так, как для того, чтобы запустить цепную реакцию по делению тяжелых ядер этого элемента, необходимо значительное количество энергии нейтронов. Уран-238 используют в качестве защиты в аппаратах деления и синтеза. Однако большая часть добытого урана-238 используется для синтеза плутония, применяемого в ядерном оружии.
Длительность периода полураспада урана ученые используют для того, чтобы рассчитать возраст отдельных минералов и небесных тел в целом. Урановые часы представляют собой достаточно универсальный механизм для подобного рода расчетов. В то же время, чтобы возраст был рассчитан более или менее точно, необходимо знать не только количество урана в тех или иных породах, но и соотношение урана и свинца как конечного продукта, в который превращаются ядра урана.
Есть еще один способ расчета пород и минералов, он связан с так называемым спонтанным Как известно, в результате спонтанного деления урана в естественных условиях его частицы с колоссальной силой бомбардируют рядом находящиеся вещества, оставляя за собой особые следы - треки.
Именно по количеству этих треков, зная при этом период полураспада урана, ученые и делают вывод о возрасте того или иного твердого тела - будь то древняя порода или относительно «молодая» ваза. Все дело в том, что возраст объекта прямо пропорционален количественному показателю атомов урана, ядра которого бомбардировали его.